Capítulo 10 - Pie diabético
10.1 Definición
El pie diabético es una alteración clínica cuya base etipatogénica es la neuropatía inducida por una hiperglicemia mantenida, en la que con o sin coexistencia de isquemia, y previo desencadenamiento traumático, se produce una lesión o ulceración del pie.
10.2 Epidemiología
La diabetes mellitus ha sido catalogada como la epidemia del siglo XXI.
Según lo datos proporcionados por la IDF (International Diabetes Federation) en 2014 se calculó que 387 millones de personas en el mundo sufrían diabetes, con una prevalencia global de 8.3%, lo que significa que 1 de cada 12 personas es diabética. Además aproximadamente un 50 % de los pacientes con diabetes están sin diagnosticar, es decir 1 de cada 2 personas con diabetes, no sabe que la padece. La diabetes fue responsable de 4.9 millones de muertes en 2014, cada 7 segundos muere una persona a causa de la diabetes. En 2014 el gasto sanitario en diabetes alcanzo un 11% del presupuesto sanitario total. Para el 2035 se calcula que la diabetes afectará a 592 millones de personas en el mundo.
La OMS maneja cifras algo inferiores estimando que en la actualidad existen 347 millones de diabéticos en el mundo (90% tipo 2 y 10 % tipo 1).
Las estimaciones previas han sido ampliamente superadas. El número anual de pacientes diabéticos está incrementándose en una proporción mucho mayor de la esperada o anticipada en años previos, así en el 2003 se estimaba que en el año 2030, la diabetes afectaría a 366 millones de personas en el mundo, es decir, las estimaciones realizadas hace tan solo 10 años para el año 2030, se han alcanzado o superado ya en la actualidad.
En España los distintos estudios realizados también indican un importante aumento de la prevalencia, pasando del 5-10% estimado hace 10 años al 10-1%5% calculado en la actualidad. Según el estudio Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo., primer estudio sobre prevalencia de la diabetes realizado a nivel nacional en España, publicado en 2011, la prevalencia global de la diabetes en España es de 13.8% (IC 95% 12.8-14.7), aproximadamente la mitad: 6% (IC 95% 5.4-6.7%) tiene diabetes no conocida. Así mismo revela que casi el 30% de la población tiene algún grado de alteración del metabolismo de los hidratos de carbono.
Este espectacular incremento de la prevalencia puede explicarse por incremento genuino en la incidencia, debido a cambios demográficos como el envejecimiento de la población, el aumento de la obesidad y del sedentarismo y a un descenso de la mortalidad en los pacientes diabéticos.
A medida que la prevalencia de la diabetes continua incrementándose, es esperable que sus complicaciones aumenten en la misma medida.
La hiperglucemia mantenida, incluso en ausencia de síntomas, conlleva lesiones en múltiples tejidos. Clásicamente las complicaciones de la diabetes se han clasificado en:
1. Complicaciones microvasculares: la microangiopatía diabética se caracteriza por una hipertrofia y proliferación de la íntima sin estrechamiento de la luz vascular que afecta a arteriolas, capilares y vénulas. Especialmente sensibles son los pequeños vasos de la retina, el riñón y los nervios periféricos:
- La retinopatía diabética es la segunda causa de ceguera en el mundo occidental y la más frecuente en personas menores de 70 años, tras 15 años con diabetes aproximadamente el 2% de los pacientes desarrollan amaurosis y el 10 % tienen severos problemas de visión.
- Nefropatía diabética: es la primera causa de insuficiencia renal en el mundo occidental, 10-20% de los diabéticos fallecen por fallo renal
- Neuropatía diabética: afecta aproximadamente al 50 % de las personas con diabetes siendo uno de los principales mecanismos fisiopatológicos en la aparición de ulceras en los pies ( con el eventual riesgo de amputación que esto conlleva).
2. Complicaciones macrovasculares: la macroangiopatía es la afectación aterosclerótica de los vasos de mediano y gran calibre. Histológicamente es similar a la de los pacientes no diabéticos pero en los diabéticos tiene un inicio más precoz, y una gravedad y extensión mayores y peor pronóstico que en el resto de la población.
- Enfermedad cardiovascular: los pacientes diabéticos tienen entre 2 y 4 veces más riesgo de ECV que la población general y entre un 50 y un 80% de las personas con diabetes mueren por ECV.
- Enfermedad cerebrovascular: dos veces más frecuente en los pacientes diabéticos que en los no diabéticos.
- Enfermedad arterial periférica: junto con la neuropatía puede contribuir a la aparición de lesiones en el pie. La afectación es típicamente multisegmentaria, bilateral y distal (lesiones principalmente a nivel infragenicular). Presente en uno de cada cuatro diabéticos, la claudicación intermitente es aproximadamente el doble de frecuente en diabéticos que no diabéticos.
3. Pie diabético: la diabetes continúa siendo la causa más frecuente de amputaciones no traumáticas en países desarrollados.
El riesgo de amputación es 15 a 40 veces mayor en pacientes diabéticos comparado con la población no diabética. El 85% de las amputaciones están precedidas de una ulcera en el pie.
El 25% de los pacientes diabéticos desarrollarán una úlcera a la largo de su vida.
La prevalencia del pie diabético está en torno a 8-13%.
Después de una amputación de una extremidad, el riesgo de nueva úlcera o amputación en la extremidad contralateral es del 50% en los 2-5 años poteriores
La mortalidad de los pacientes amputados es del 50% a los 3 años.
Las lesiones en el pie, constituyen la causa más frecuente de hospitalización de los pacientes diabéticos (20-30%) con estancias prolongadas.
El 20% del gasto total en diabetes sería atribuible al pie diabético en los países desarrollados.
________________________________________
10.3 Fisiopatología
El conocimiento de la fisiopatología del pie diabético es esencial, pues modificando los factores que influyen en su desarrollo se puede restaurar o mantener el pie intacto.
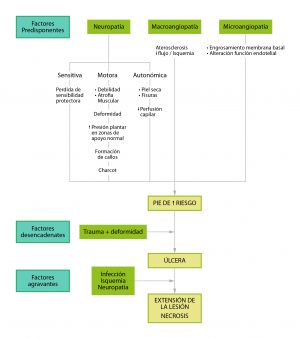
De forma esquemática, en la fisiopatología evolutiva del pie diabético deben considerarse tres tipos de factores: los predisponentes, que sitúan a un enfermo diabético en situación deriesgo de presentar una lesión, los desencadenantes o precipitantes, que inician la lesión y los agravantes o perpetuantes, que retrasan la cicatrización y facilitan las complicaciones
10.3.1 Factores Predisponentes
Neuropatía
La neuropatía con o sin isquemia asociada esta implicada en la fisiopatología del pie diabético entre el 85 y 90% de los casos.
Aunque solo un 10-15% de los enfermos manifiestan síntomas, la disminución de la velocidad de conducción nerviosa es evidenciable hasta en el 80% de los pacientes. Su prevalencia está en relación con el grado de control metabólico y los años de evolución de la enfermedad. La forma más frecuente de neuropatía es la polineuropatía simétrica distal, que afecta tanto a fibras somáticas (sensitivas y motoras) como autonómicas, predominantemente de miembros inferiores.
Neuropatía sensitiva: con afectación de la sensibilidad profunda (perdida del sentido de la posición, sensibilidad vibratoria..) y superficial (táctil, térmica y dolorosa), Debido a ella, los diabéticos no son capaces de detectar cambios de temperatura, exceso de presión o traumatismos debidos al calzado…
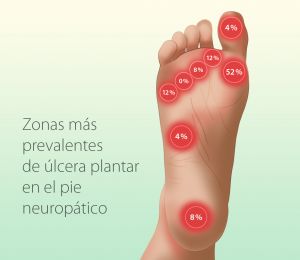
Neuropatía motora: provoca atrofia y debilidad de la musculatura intrínseca del pie, provocando acortamientos tendinosos y dando lugar a la deformidad del mismo y una distribución anormal de las cargas en el pie favoreciendo la aparición de ulceras. Las más frecuentes son los dedos en martillo y en garra con protrusión de la cabeza de los metatarsianos.
Fig. 1 Zonas de apoyo plantar
Contribuye a esta deformidad del pie la glicosidación del colágeno que va a dar lugar al endurecimiento y rigidez de la capsulas articulares y ligamentos causando limitación de la movilidad articular y una piel gruesa y firme.
Neuropatía autonómica: provoca anhidrosis dando lugar a una piel seca que facilita la a aparición de fisuras que pueden ser el inicio de úlceras o actuar como puerta de entrada para los microorganismos. También provoca la apertura de shunts arterio-venosos cutáneos provocando la disminución de la perfusión capilar, aumento de temperatura, edema y alterando la respuesta inflamatoria normal a la agresión.
La conjugación de todos estos factores en los estadios más avanzados (en asociación con un insulto traumático) es lo que determina la aparición de la neuroartropatía de Charcot. Menos del un 1% de los diabéticos desarrollaran esta grave complicación, caracterizada por dislocación de articulaciones del pie, fracturas patológicas y destrucción severa de la arquitectura del pie de la que más tarde hablaremos
Macroangiopatía
La isquemia está implicada en el 40-50% de los casos, generalmente asociada a neuropatía. Como se ha mencionando anteriormente la aterosclerosis en los pacientes diabéticos es más precoz, rápida y extensa que en la población general y la afectación en los miembros inferiores es típicamente bilateral, multisegmentaria y distal
Microangiopatía
Se caracteriza por hipertrofia y proliferación de la íntima con engrosamiento de la membrana basal pero sin estrechamiento de la luz vascular que genera alteraciones funcionales en la microcirculación. Existe una gran controversia sobre la importancia real de la microangiopatía en la fisiopatología del pie diabético, parece tener un papel secundario y todavía incierto en la aparición de úlceras en el pie, es posible que contribuya en tanto en cuanto disminuye la respuesta vasodilatadora a estímulos con disminución de la respuesta inflamatoria a traumatismos o infección.
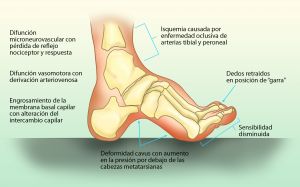
Fig. 2 Alteraciones pie diabético
Las úlceras más frecuentes son la neuropáticas de un 45-60%, seguidas de las neuroisquémicas 25-45%, mientras que las puramente isquémicas solo constituyen el 10-15%
10.3.2 Factores Desencadenantes
Traumatismos
Los traumatismos pueden ser:
- Mecánicos: es el factor precipitante más frecuente, aunque puede ser el resultado de una lesión directa punzante o penetrante (como lesiones producidas al pisar una chincheta, clavo, cristal..); generalmente son causadas por el traumatismo repetido ocasionado por calzados mal ajustados o demasiado apretados sobre prominencias óseas ( dedo martillo, hallux valgus, aspectos lateral, medial y dorsal del pie…). En la planta del pie estas lesiones aparecen sobre zonas que debido a su deformidad reciben una alta presión con el apoyo: cabeza de metatarsiano, equino, Charcot,… donde aparecen zonas de hiperqueratosis (callosidades), ampollas o úlceras debidas simplemente a la presión normal, moderada pero reiterativa que supone la deambulación.
La principal causa de lesiones en el pie diabético el traumatismo causado por el calzado en el contexto de una perdida de la sensibilidad protectora y en presencia de deformidad del pie.
- Térmicos: lesión directa en la piel por calor o frío, por ejemplo al meter el pie enagua demasiado caliente, acercarlo demasiado a una fuente de calor…etc.
- Químicos: suelen producirse por aplicación inadecuada de agentes queratolíticos como el ácido salicílico.
Deformidad del pie
Las deformidades condicionan una aumento de presión sobre la zona, provocando la aparición de callosidades, que constituyen lesiones pre ulcerosas, ya que hasta un 50% de las úlceras se inician sobre estas lesiones.
10.3.3 Factores Agravantes
Infección
La infección no suele ser la causa de la úlcera (excepto en los casos de infecciones fúngicas como la tinea pedis o la candidiasis en los espacios interdigitales), sin embargo, va a determinar en gran medida tanto el tratamiento como el pronóstico de cualquier lesión en el pie.
Los diabéticos como consecuencia de las alteraciones metabólicas presentan una alteración de la respuesta inmunitaria que los hace más vulnerables a la infección. afecta sobre todo a los granulocitos alterando su estructura y función (quimiotaxis, diapédesis, fagocitosis…).
Las úlceras suelen estar sobre infectadas por microorganismos diversos, que en su mayoría son saprófitos (estafilococos y estreptococos), aunque también pueden detectarse aerobios y anaerobios facultativos como el E. Coli o anaerobios estrictos (bacteroides y clostridium), frecuentemente son polimicrobianas.
Neuropatía
La pérdida de sensibilidad provocada por la neuropatía impide al paciente reconocer la lesión y permite que camine sobre tejidos infectados sin ser consciente de ello, facilitando la difusión de la infección a planos más profundos e incrementando su gravedad.
Isquemia (macroangiopatía)
Disminución del flujo sanguíneo y de la presión de perfusión en la circulación distal, disminuyendo el aporte de oxígeno y nutrientes que puede ocasionar necrosis, disminuir la capacidad de cicatrización y agravar la infección favoreciendo el crecimiento de anaerobios por el ambiente hipóxico, disminuyendo la llegada de antibiótico a la lesión.
10.4 Clínica
10.4.1 Neuropatía
La forma más frecuente de afectación es la neuropatía simétrica distal. En la mayoría de los casos los síntomas leves o nulos y la presencia de neuropatía se detecta en el momento del examen físico.
En etapas tempranas se evidencia pérdida de reflejos osteotendinosis, alteración de la sensibilidad vibratoria y pérdida simétrica y distal de la sensibilidad cutánea, incluyendo temperatura, tacto fino y dolor.
El inicio suele ser insidioso y bilateral con parestesias y dolor localizado en la región distal en forma de guante o calcetín, es descrito como urente, quemante, fulgurante y empeora durante el reposo. En las formas más dolorosas existe hiperestesia que hace intolerable el roce de la ropa o de las sábanas.
La pérdida de la sensación de dolor y temperatura da lugar a úlceras penetrantes indoloras y lesiones tróficas en los pies. La pérdida de la posición articular y sensación de dolor profundo pueden ocasionar artropatía neuropática (Charcot) que afecta principalmente a las articulaciones del tarso y metatarso.
La afectación motora dará lugar a las deformidad del pie por atrofia de la musculatura intrínseca del mismo: dedos en martillo…etc.
10.4.2 Isquemia
Las manifestaciones clínicas de la isquemia presentan la particularidad de que al estar asociados en la mayoría de las ocasiones a la neuropatía, pueden estar modificados (minimizados o magnificados) por esta.
Puesto que la diabetes afecta fundamentalmente a arterias infrainguinales, la claudicación intermitente a nivel soleogemelar es la forma de presentación más frecuente. La claudicación plantar es sin embargo menos prevalente, dado que la escasa masa muscular del pie, muchos autores sostienen que el pie no tiene capacidad para presentar claudicación, y muchos pacientes diabéticos presentan úlceras isquémicas sin haber padecido claudicación. La clínica no se diferencia de la de pacientes no diabéticos, manifestándose como dolor, calambres o fatiga muscular que aparecen con la deambulación y ceden al detenerse, la distancia de claudicación siempre es constante, acortándose en pendientes, al caminar más rápido o con el frío. Hay que hacer diagnóstico diferencial con otros procesos que también se manifiestan con dolor con la deambulación como la artrosis, radiculopatías, estenosis del canal raquídeo…etc.
En fases avanzadas aparece el dolor en reposo, caracterizado por la presencia de dolor aún en ausencia de ejercicio. Suele exacerbarse por las noches debido al decúbito y a la disminución de la presión arterial que se produce fisiológicamente durante el sueño. El dolor se localizada en las regiones más distales como los dedos y mejora con la sedestación, la bipedestación y al dar unos pasos (ya que se incrementa el gasto cardiaco, pero empeora si persiste el ejercicio a diferencia del dolor neuropático que mejora al caminar).
La sensación de frialdad en el pie puede estar presente tanto en el pie isquémico como el neuropático, sin embargo el pie isquémico estará frío a la palpación mientras que el neuropático no.
La palidez del pie y el retraso en el relleno venocapilar son otros signos de isquemia. La palidez se incrementa con la elevación del pie adquiriendo un rubor intenso (eritromelalgia) al pasar a la posición declive.
Suele existir atrofia cutánea, con piel fina con pérdida del vello de los dedos y del dorso del pie. Se evidencia también engrosamiento de las uñas que a menudo muestran sobreinfección por hongos.
Las lesiones isquémicas son muy dolorosas, localizadas en la regiones distales de los dedos, cara medial de la cabeza del primer metatarsiano o superficie lateral de la cabeza del quinto metatarsiano y en el talón. Sin embargo, los pacientes que asocian neuropatía, el dolor puede estar enmascarado y pueden presentar lesiones isquémicas indoloras o úlceras neuropáticas en zonas de apoyo plantar cuya cicatrización fracasa debido a la isquemia. La piel perilesional suele presentar un aspecto eritematoso debido a la vasodilatación capilar refleja, la cual se diferencia de la celulitis en que desaparece al elevar el pie.
10.4.3 Infección
Cuando las lesiones se sobreinfectan, la evolución es rápida, tórpida y aparece exudado, supuración, edema y eritema por la celulitis asociada y, si la infección progresa por los vasos linfáticos, pueden aparecer líneas eritematosas que ascienden por el dorso del pie y la pierna (linfangitis).
El paciente puede presentar fiebre, afectación del estado general y glucemias elevadas de difícil control.
La infección puede complicar tanto lesiones neuroisquémicas como neuropáticas. En estas últimas, se pueden observar necrosis digitales con pulsos distales conservados, esta necrosis no es debida a la microangiopatía como antiguamente se pensaba, si no a la trombosis capilar causada por toxinas necrotizantes liberadas por diferentes bacterias.
Una forma muy agresiva de infección es la infección necrotizante de tejidos blandos que suele estar causada por flora polimicrobiana, causando una necrosis extensa de los tejidos profundos, en ocasiones con formación de abscesos y crepitación.
Para realizar un correcto examen de la úlcera hay que desbridar todas las callosidades y el tejido necrótico, debe valorarse la profundidad, si a través de la lesión con un objeto estéril se llega al hueso, debe asumirse la presencia de osteomielitis, con un valor predictivo del 89%, si el hueso está totalmente expuesto, la certeza diagnostica es del 100%. No es infrecuente que una úlcera inicialmente de aspecto reducido, derive una vez desbridada en una extensa necrosis.
10.5 Clasificación de las Lesiones del Pie Diabético
Existen numerosas clasificaciones tanto fisiopatológicas como clínicas, en función de criterios tales como la presencia o ausencia de isquemia, el grado de la misma, gravedad de la infección, extensión de la pérdida tisular…etc.
10.5.1 Clasificación de Edmonds
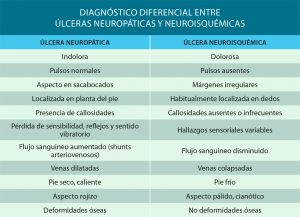
Es una clasificación basada en la fisiopatología que diferencia entre úlceras neuropáticas no isquémicas y úlceras de etiología isquémica, existiendo frecuentemente una superposición entre ambas
Úlcera neuropática
- Pulsos presentes.
- Indolora.
- Sobre zonas de presión (generalmente en la planta del pie, es el denominado mal perforante plantar).
- Hiperqueratosis cutánea (suele estar rodeada de tejido calloso, como un cráter).
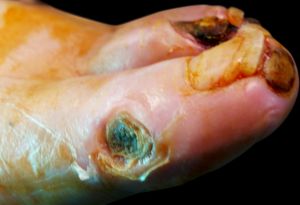
- Índice tobillo-brazo > 1.1.
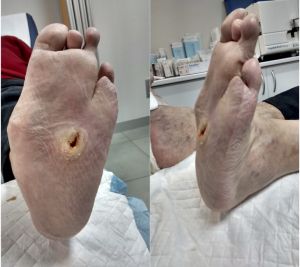
Fig. 3 Mal perforante plantar
Úlcera neuroisquémica
- Pulsos negativos
- Dolorosas
- Distales (generalmente en los dedos)
- Mínimo tejido de granulación
- Índice tobillo-brazo < 1.1
Fig. 4 Úlcera neuroisquémica
10.5.2 Clasificación de Wagner
Es la clasificación más ampliamente aceptada, establece seis categorías o grados basándose en la profundidad de la lesión y la extensión de la infección o necrosis.
Grado 0: Piel íntegra, sin lesiones. Puede haber deformidad o celulitis.
Se trata del pie en riesgo, puede existir zonas potenciales de úlcera, como dedos en martillo, hallux valgus, Charcot, hiperqueratosis, isquemia,...pero sin lesiones.
Grado 1: Úlcera superficial.
Grado 2: Úlcera profunda no complicada (afectación del tendón, capsula articular o hueso)
Grado 3: Úlcera profunda complicada (hay absceso, osteomielitis o artritis séptica)
Grado 4: Gangrena localizada (antepié o talón)
Grado 6: Gangrena de todo el pie.
Esta clasificación aunque sencilla no considera aspectos fundamentales como el grado de isquemia y no consigue en ocasiones una descripción precisa y clara de las lesiones, sin embargo resulta lo suficientemente adecuada para establecer algoritmos para el tratamiento.
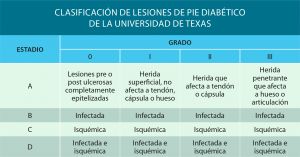
10.5.3 Clasificación de Texas
Es una clasificación más completa que las anteriores, ha sido validada y junto a la de Wagner es la más utilizada.
Relaciona profundidad de la lesión (grados 0-III) con isquemia e infección (estadios A-D, A: no infección ni isquemia; B: infección sin isquemia, C: isquemia sin infección; D: infección e isquemia). Conforme aumenta el grado y el estadio es menos probable que la lesión cure sin necesidad de revascularización o amputación.
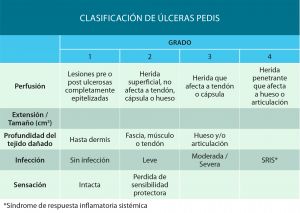
10.5.4 Sistema PEDIS
Evalúa cinco características: perfusión, extent/size, depth/tissue loss, infection y sensation, asignando a cada uno de ellos distintos grados. Este sistema fue desarrollado por el IWDFG (Internacional Working Group on the Diabetic Foot) con el objetivo de aunar criterios que hiciesen posible la comunicación científica en el ámbito de la investigación. Es un sistema complejo que requiere el uso de pruebas diagnosticas complementarias, aporta una gran cantidad de información, pero su uso en la practica clínica es complicado.
10.5.5 Sistema de clasificación S(AD) SAD
Recibe su nombre del acrónimo en inglés S(AD) size(Ambi/depth), SAD sepsis, arteriopathy, denervation. Relaciona el tamaño de la lesión teniendo en consideración el área y la profundidad, con la presencia de infección, arteriopatía y neuropatía, graduando cada parámetro de 0 a 3 de menor a mayor gravedad.
10.5.6 Sistema DUSS (Diabetic Ulcer Severity Store)
Es un sistema extremadamente sencillo que evalúa sólo la existencia o no de cuatro parámetros, asignando 1 punto si se da dicho parámetro y 0 si no se da: ausencia de pulsos distales (1 punto), sondaje al hueso positivo (1 punto), úlcera localizada en cualquier parte del pie distinta de los dedos (1 punto) y existencia de más de una úlcera (1 punto).
Es un sistema muy útil para evaluar la gravedad de las lesiones, probabilidad de curación de las mismas, necesidad de derivar al especialista..
Existen otros muchos sistemas, la mayoría incluyen parámetros para evaluar la infección, la isquemia y la profundidad, su aplicación varía en función del ámbito asistencial donde va a ser utilizado, sistemas sencillos y ámbito de utilizar resultan útiles en el ámbito de la atención primaria, en atención especializada o para la investigación sistemas mas detallados como el de Texas, PEDIS, SAD resultan más adecuados.
10.6 Diagnóstico
10.6.1 Historia clínica
Se debe realizar una historia clínica completa del paciente que recoja no solo datos sobre la diabetes (duración, control glucémico, tratamiento), también todas las patologías que presente o haya presentado el paciente, haciendo especial hincapié en aquellas patologías que puedan influir en el curso de la diabetes o puedan ser causadas por ella. Se debe preguntar activamente por la existencia de otros factores de riesgo vascular (HTA, DL, tabaquismo), enfermedad cardiovascular o renal, existencia de claudicación o dolor en reposo, presencia de síntomas neuropáticos (disestesias, parestesias en calcetín…). Si existe lesión habrá que indagar sobre cual fue el mecanismo desencadenante, tiempo de evolución, si ha recibido tratamiento antibiótico previo, si ha tenido otras lesiones previas que hayan requerido amputación o hospitalización…etc.
10.6.2 Exploración física
Además de la exploración general del paciente, se debe de realizar el examen sistemático de las extremidades inferiores. Este examen debe realizarse una vez al año en pacientes diabéticos y más a menudo si presentan alguna complicación en el pie.
Exploración basal del pie
Valoración dermatológica: se debe examinar el aspecto de la piel (color, textura, temperatura, edema…) evaluando la presencia de sequedad (anhidrosis), hiperqueratosis o callosidades, ausencia de vello, presencia de fisuras o grietas, alteraciones ungueales (hipertrofia, atrofia, onicomicosis, paroniquia..), presencia de lesiones (localización, tamaño, profundidad, infección, necrosis..). Hay que contemplar siempre la posibilidad de la existencia de osteomielitis asociada a la lesión, en ocasiones esta se asocia a una importante afectación de partes blandas que pueden estar limitadas, por ejemplo a un dedo (que aparecerá tumefacto, eritematoso, caliente: dedo en porreta) o a todo el pie ( en cuyo caso hay que hacer el diagnóstico diferencial con neuroartropatía de Charcot). Pero en otras ocasiones la presentación es subaguda o crónica, con formación de fístulas que comunican el hueso o la articulación con la piel y con escasa reacción inflamatoria asociada. Clásicamente se ha considerado que la palpación del hueso con un estilete a través de la úlcera tenia un valor predictivo positivo de diagnóstico de osteomielitis del 89%, sin embargo, estudios más recientes han hallado que el valor predictivo positivo es menor (53-57%), sin embargo un resultado negativo tiene un alto valor predictivo negativo (98%) que prácticamente descarta el diagnostico.
Valoración osteoarticular
Presencia de deformidades: dedo en martillo o en garra, hallux valgus, pie cavo o plano, atrofia de la musculatura (subluxación metatarso falángica), deformidad de Charcot, limitación de la movilidad articular (la dorsiflexión del pie debe ser mayor de 10 grados para permitir una marcha normal, mas de la mitad de los pacientes diabéticos presenta valores inferiores), amputaciones previas…etc.
Exploración neurológica
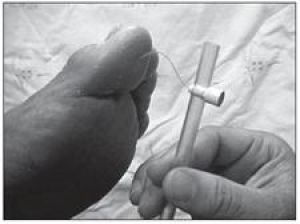
Sensibilidad vibratoria: se explora en la epífisis distal de primer metatarsiano mediante un diapasón o un biodensiómetro (este último algo más preciso). Predice el riesgo de ulceración con una sensibilidad del 80% y una especificidad del 60%.
Sensibilidad táctil ligera (test de presión fina): se explora con el monofilamento de Semmes-Weinstein de 10 g, se trata de un filamento de nylon que se aplica sobre la piel presionando hasta que se curve ligeramente, preguntando al enfermo si percibe el contacto. No existe un consenso sobre las zonas a explorar pero la mayoría de los autores están de acuerdo con explorar a nivel plantar de la cabeza del primer, tercer y quinto metatarsianos, dedos primero y quinto, talón y en la porción proximal de la cara dorsal entre el primer y segundo dedos. Su sensibilidad para el diagnostica de neuropatía es el 95-100%. Un test positivo incrementa el riesgo de ulceración 10 veces y el de amputación 17 veces.
Fig. 5 Test de sensibilidad fina
Valoración del reflejo aquíleo: su negatividad indica pérdida de la sensibilidad propioceptiva
Exploración vascular
Palpación de pulsos: se deben palpar los pulsos femoral, poplíteo, tibial posterior y pedio en ambas extremidades
Soplos: en el sector aorto-iliaco y femoral, que indican la existencia de una estenosis a estos niveles.
Temperatura: en ambas extremidades valorando su simetría
Coloración: palidez, cianosis, eritromelalgia de decúbito
Relleno venocapilar.
La exploración vascular del pie debe completarse con un estudio hemodinámico, (ITB, presiones parciales y pletismografía, presión digital, presión transcutánea de oxígeno), y esto es preceptivo si la historia o la exploración física sugieren isquemia o existe una lesión que no cura.
10.6.3 Pruebas complementarias
Exámenes de laboratorio
Analítica:hemograma, bioquímica que incluya glucemia, creatinina, urea, iones, hemoglobina glicosilada, PCR, VSG, PTC (procalcitonina). En caso de infección de la lesión puede ser difícil conseguir un adecuado control glucémico, y la glucosa permanece elevada en sangre incluso con terapia intensiva con insulina hasta que la infección sea controlada. La PCR, la VSG y la PTC son marcadores serológicos de inflamación que resultan de utilidad para valorar la gravedad de la infección y valorar la respuesta al tratamiento antibiótico.
Cultivo de la herida: sólo ha de realizarse cuando se sospecha infección (es decir en presencia de signos clínicos de infección, pues invariablemente todas las úlceras van a estar colonizadas por bacterias, y su aislamiento puede llevar a instaurar tratamientos antibióticos no necesarios, generando la aparición de resistencias). Siempre que sea posible debe ser recogido antes de iniciar el tratamiento antibiótico. Antes de la toma se debe desbridar la úlcera y limpiar la misma. La muestra se debe obtener del fondo de la úlcera y siempre que sea posible es preferible la toma de biopsia ya que las muestras titulares proporcionan resultados mas fiables que las recogidas con torunda.
Cuando se sospecha osteomielitis, la biopsia ósea permite confirmar el diagnóstico, sin embargo sólo estaría indicada si el diagnóstico de imagen es dudoso.
Hemocultivos: si existe fiebre mayor o igual a 38 ª o afectación sistémica.
Exploración vascular
Índice tobillo-brazo (ITB): como se menciona anteriormente, debe ser sistemáticamente realizado en todos los pacientes diabéticos. Los valores normales se oscilan entre 0.9 y 1.2. Un ITB inferior a 0.9 es indicativo de enfermedad arterial periférica. Un índice inferior a 0.3 indica isquemia crítica. Los diabéticos debido a la calcificación de la capa media que impide la compresión arterial, pueden tener valores de ITB falsamente elevados, debe sospecharse este hecho cuando el índice es igual o mayor a 1.3 (en algunos casos ni siquiera es posible colapsar la arteria).
La medida de la presión digital en el primer dedo (donde excepcionalmente se produce calcificación arterial) y de la presión transcutánea de oxígeno (TcPO2, medida indirecta de la cantidad de oxígeno que llega a la piel) constituyen métodos alternativos al ITB cuando se sospecha que el resultado de este puede estar alterado por la calcificación arterial, mediciones inferiores a 25 mmHg de TcPO2 o de 30 mmHg en el dedo son predictivos de no cicatrización de la lesión.
Presiones parciales segmentarias y examen de la onda del pulso: Utilizando manguitos de presión en distintos sectores de la extremidad permiten localizar el nivel de la oclusión y la severidad de la misma, que vendría determinado por la severidad y localización de la caída de presión y del aplanamiento de la onda del flujo.
La ecografía doppler, la angioTAC, la angioRNM y la angiografía, son métodos de exploración morfológica que permiten establecer la topografía lesional y son utilizados para planificar la estrategia quirúrgica si se va a realizar revascularización. Tanto la RM como el TC proporcionan una información limitada en vasos de pequeño calibre (como las arterias infrapoplíteas y en presencia de calcificación arterial, lo cual hace necesario en muchas ocasiones la realización de la arteriografía.
Estudios de imagen
En el pie diabético se pueden producir alteraciones osteoarticulares debido tanto a infecciones como a procesos no infecciosos. En ocasiones resulta difícil la interpretación de los estudios de imagen y es complicado diferenciar entre una osteomielitis y alteraciones debidas a la neuroartropatía, por ello todos los estudios de imagen deben interpretarse en conjunto con los hallazgos clínicos.
Radiografía simple: debe de ser el estudio de imagen inicial en todos los pacientes con pie diabético. Puede detectar osteítis (desestructuración de la cortical), osteomielitis (destrucción trabecular, imágenes de secuestro con reacción perióstica circundante..), gas en el tejido celular subcutáneo, cuerpos extraños…, así mismo evidencia deformidades estructurales del pie, calcificación arterial o dislocaciones y fracturas propias de la neuroartopatía de Charcot.
Los cambios óseos producidos por la osteomielitis no son evidenciables en la radiografía hasta pasadas las dos o tres primeras semanas, por lo que la radiografía en las fases iniciales puede ser normal.
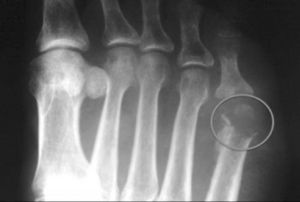
Fig.6 Osteomielitis cabeza de 5º metatarsiano con destrucción ósea a este nivel
Resonancia magnética: es la técnica de imagen más útil para el diagnóstico de osteomielitis, sería la técnica de elección ante la sospecha de osteomielitis con una radiografía normal. Permite tanto la valoración del hueso como la afectación de partes blandas. Sin embargo no siempre permite distinguir entre infección y neuroartopatía de Charcot.
Tomografía axial computerizada: puede ser una alternativa a la RM, cuando esta no puede realizarse o por razones de efectividad (mayor disponibilidad, menor coste…).
Gammagrafía con leucocitos marcados: permite realiza el diagnostico de osteomielitis y realizar el diagnóstico diferencial con osteoartropatía de Charcot. Se puede solicitar cuando existen dudas diagnósticas.
PET: también permite realizar el diagnóstico diferencial entre estas dos patologías con una alta sensibilidad y especificidad, pero su accesibilidad es menor.
10.7 Tratamiento
El principal objetivo del tratamiento es obtener el cierre de la herida tan rápidamente como sea posible. Solucionar las lesiones y disminuir su recurrencia disminuye la probabilidad de amputación del paciente diabético.
10.7.1 Manejo de las comorbilidades
Se debe conseguir un adecuado control de todas las patologías que puedan influir en el curso de la diabetes o puedan estar causadas por ella y/o puedan influir en la cicatrización de la lesión.
El control glucémico es fundamental para disminuir las complicaciones, el objetivo es mantener valores de Hbc < 6.5%.
Es preceptiva la supresión tabáquica, ya que el tabaco es un potente vasoconstrictor y disminuye el aporte de oxígeno a la lesión.
Los valores de tensión arterial deben mantenerse por debajo de 130/85 mmHg y los de LDL en menos de 100 mg/dl.
Así mismo se debe controlar la cardiopatía isquémica, la insuficiencia renal…
10.7.2 Manejo de la lesión
El tratamiento va a variar dependiendo de la severidad de la lesión.
En las lesiones superficiales la limpieza de la herida empleando suero con una solución antiséptica (povidona yodada jabonosa, clorhexidina..) suele ser suficiente.
Se debe desbridar el tejido necrótico, infectado, esfacelos y fibrina, así como el tejido calloso que rodee la ulcera si lo hubiese. La úlcera no va a curar en presencia de tejido inviable, así el desbridamiento cumple varias funciones: permite la evaluación del lecho de la lesión y de posibles trayectos o fístulas hacia estructuras más profundas o proximales, evita la progresión de la infección al disminuir la carga bacteriana y facilita el drenaje de material purulento, estimula el crecimiento de tejido de granulación y disminuye la presión.
El desbridamiento ha de ser tan extenso como sea necesario (tanto en profundidad como en superficie) hasta que se alcance tejido sano, viable y sangrante. Esto es especialmente importante en infecciones graves (abscesos, fascitis necrotizante, gangrena gaseosa…), pues muchas veces la viabilidad del pie e incluso la vida del paciente dependen de un desbridamiento agresivo que en la mayoría de las ocasiones implica amputaciones digitales. Durante el desbridamiento deben obtenerse muestras tisulares para el cultivo.
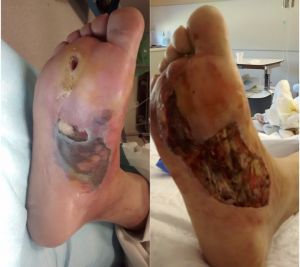
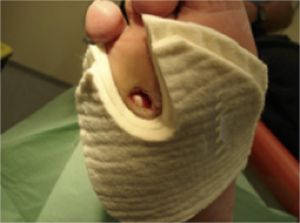
Fig. 7 Necrosis y desbridamiento plantar
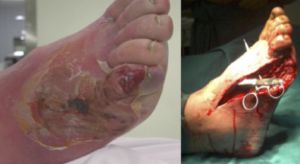
Fig. 8 Necrosis 5º dedo y tarso. Amputación y desbridamiento
El desbridamiento se repetirá tan frecuentemente como sea necesario si se sigue evidenciando la presencia de tejido necrótico o desvitalizado.
En lo anteriormente mencionado hay que hacer la excepción de las úlceras isquémicas donde el desbridamiento suele estar contraindicado hasta que no se revasculariza la extremidad (pues solo conduciría a la formación de nuevo tejido necrótico) salvo que exista infección, entonces se realizara un desbridamiento conservador, drenando el absceso pero dejando las zonas dudosas para eliminarlas posteriormente, una vez realizada la revascularización.
Las infecciones muy graves (gangrenas extensas, fascitis necrotizantes..) generalmente van a precisar una amputación mayor de entrada.
Una vez desbridada y limpiada la herida se dejará una cura que mantenga la humedad de la herida y favorezca la granulación, la cura ha de ser oclusiva para evitar la sobreinfección, generalmente con un vendaje suave. De los múltiples productos que se utilizan para curar las úlceras (pomadas con povidona, colágeno, desbridantes enzimáticos, antibióticos, apósitos con plata, suero hipertónico…), no hay evidencia de la superioridad de unos sobre otros, por lo que la elección debe basarse en las indicaciones clínicas y en la experiencia del profesional).
En la úlceras infectadas o isquémicas en cambio se debe realizar una cura seca ( povidona solución, gasas secas) hasta que se trate la infección o sean revascularizadas, ya que una cura húmeda generaría un ambiente macerado que promueve el crecimiento bacteriano.
El cierre se produce generalmente por segunda intención, a veces se utilizan dispositivos de vacío para acelerar la cicatrización o se realizan injertos cutáneos si el defecto es amplio.
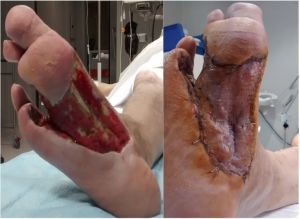
Fig. 9 Desbridamiento plantar y posterior injerto cutáneo
10.7.3 Tratamiento de la Infección
El tratamiento antibiótico estará indicado sólo si existen criterios clínicos locales o sistémicos de infección.
Inicialmente se instaurará un tratamiento empírico, la elección del mismo dependerá de cual sea la etiología más probable, lo cual a su vez estará condicionado por varios factores: gravedad de la infección, tiempo de evolución de la lesión y la posible existencia de resistencias bacterianas.
En la elección del tratamiento hay que tener en cuenta además que la peor respuesta a la infección de los pacientes diabéticos, condicionada por la alteración de la respuesta inmune y la posible isquemia asociada (que dificultará la llegada del antibiótico a la lesión), por lo cual se recomienda el uso de antibióticos bactericidas, durante largo tiempo y a altas dosis. También hay que considerar el posible deterioro de la función renal que pueden presentar estos pacientes, por lo que se evitarán el lo posible los fármacos nefrotóxicos (aminoglucósidos, vancomicina…).
Los cocos Gram positivos (y especialmente S. Aureus) son los patógenos predominantes en cualquier circunstancia, por lo que siempre deben de ser cubiertos.
Las infecciones superficiales y recientes suelen ser monomicrobianas y las especies más aisladas son S. Aureus y estreptococos. Sin embargo, a medida que aumenta la cronicidad o la gravedad, la complejidad de la flora aumenta y las infecciones suelen ser polimicrobianas y mixtas, por lo que además de estafilococos y estreptococos, se encuentran otros como enterococos, enterobacterias, Pseudomona, anaerobios… Los tratamientos antibióticos y los ingresos previos también contribuyen a la selección de este tipo de microorganismos, así como a la aparición de resistencias. Debemos considerar SARM (S.Aureus meticilin resistente) si el paciente ha estado hospitalizado durante el último año, si ha recibido tratamiento con quinolonas en los últimos meses, si ha presentado infección previa por SARM, si la prevalencia de infección por SARM en el centro hospitalario es mayor del 10%...etc.
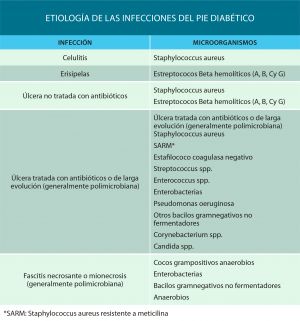
En la siguiente tabla se exponen los microorganismos más frecuentes en función de la gravedad de la infección, tiempo de evolución y la existencia de tratamiento antibiótico previo.
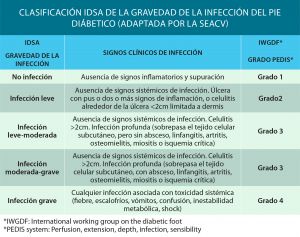
La clasificación más ampliamente utilizada para valorar la severidad de las infecciones en el pie diabético es la de la IDSA (Infectious Disease Society of América) incorpora además al grado de severidad según el sistema PEDIS.
En esta clasificación los signos de toxicidad sistémica son utilizados como marcadores de gravedad, sin embargo hay que tener en cuenta que debido al estado de inmunosupresión asociado a la diabetes, mas del 50% de los pacientes con infecciones graves no presentan signos de sistémicos de infección, y por tanto la ausencia de estos no excluye la misma, la fiebre y la leucocitosis pueden estar ausentes y a veces el único signo es una hiperglucemia incontrolable.
La gravedad de la infección determina el pronóstico y la estrategia terapéutica. A efectos prácticos, lo importante es saber que infecciones pueden ser tratadas de modo ambulatorio con seguridad y cuales precisan ingreso hospitalario y tratamiento intravenoso porque suponen un riesgo para la extremidad o la vida del paciente.
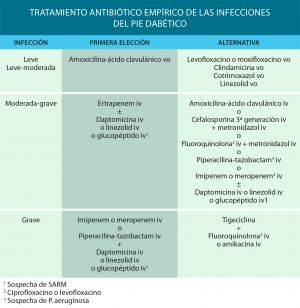
Infecciones leves e infecciones leves-moderadas (no hay amenaza de pérdida de extremidad). Úlceras sin isquemia significativa, sin afectación de hueso, músculo ni articulación ni absceso profundo. Pueden tratarse de forma ambulatoria con antibiótico oral durante 1-2 semanas. Hay que cubrir Gram positivos (etiología principal), teniendo en cuenta que también pueden estar implicados Gram negativos. El antibiótico de elección es la amoxicilina-clavulánico, y en caso de sospecha de SARM o ECN (estafilococos coagulasa negativo: S. Epidermidis) cotrimoxazol o linezolid. En pacientes alérgicos a betalactámicos puede utilizarse levofloxacino, moxifloxacino, clindamicina o cotrimoxazol. Se debe revisar al paciente a las 48-72 horas, si no se ha producido mejoría hay que plantearse la hospitalización.
Infección moderada-grave (riesgo de pérdida de extremidad). Hospitalización y tratamiento antibiótico de amplio espectro de 2 a 4 semanas. Los antibióticos deben ser activos frente a cocos Gram positivos aerobios (Staphylococcus spp y Streptocooccus spp), bacilos gran negativos (enterobacterias) y anaerobios (Streptococcus spp, Peptostreptococcus spp y Bacteroides spp). Ertapenem parece la primera opción por via parenteral (una sola dosis diaria, penetra bien en los tejidos, activo frente a E. Coli productor de betalactamasas..). Si se sospecha P. Aeruginosa se utilizará piperacilina-tazobactam o un carbapenem anti pseudomónico. Se debe asociar daptomicina, linezolid o vancomicina (si no hay insuficiencia renal) si existe alta probabilidad de SARM.
Infección grave (amenaza la vida). Se deben cubrir todas las posibilidades etiológicas con betalactámicos con actividad antipseudomona (carbapenems o piperacilina-tazobactam) asociados a daptomicina, linezolid o vancomicina. En caso de alergia a betalactámicos, se usará tigeciclina asociada a quinolona o amikacina.
Una vez conocido el agente causal y su sensibilidad se ajustará el tratamiento antimicrobiano.
10.7.4 Tratamiento de la isquemia.
Tratamiento médico de la isquemia.
No difiere del tratamiento empleado en el enfermo no diabético con enfermedad arterial periférica: control estricto de los factores de riesgo cardiovascular, antiagregación, ejercicio, Cilostazol…
La medicación antiagregante (AAS, Clopidogrel..) presenta un efecto beneficioso sobre la disminución de la mortalidad cardiovascular, la permeabilidad de la cirugía revascularizadora y la progresión de la aterosclerosis, sin embargo, no existe evidencia de que estos fármacos mejoren la evolución de la isquemia crítica, por lo que en presencia de lesiones isquémicas o neuroisquémicas, es difícil que el tratamiento médico aislado de la isquemia sea suficiente para la cicatrización de la lesión (salvo en grados leves de isquemia).
Control del dolor
La isquemia crítica produce un dolor intenso, de difícil control, en ocasiones incoercible. Lo ideal es que el control del dolor se consiga mediante la revascularización de la extremidad, pero hasta que esta se realice, o en aquellas ocasiones en las que no es posible realizarla, es esencial conseguir el alivio del dolor del paciente. Para ello se utiliza analgesia de forma pautada y de potencia creciente, se suelen utilizar combinaciones de fármacos (por ejemplo paracetamol y metamizol), hay que tener cuidado con los AINES ya que a menudo estos pacientes presentan insuficiencia renal e HTA. A menudo es necesario el uso de opioides (tramadol, fentanilo..)
Revascularización
Debe plantearse la revascularización si existen signos claros de isquemia crítica y cuando no se consigue la cicatrización de la úlcera neuroisquémica a pesar del tratamiento médico óptimo ( cuidados de la herida, tratamiento de la infección si la hubiese y descarga).
Como se ha mencionado anteriormente, la enfermedad arterial periférica en el paciente diabético se caracteriza por la afectación difusa y segmentaria de los vasos distales. Sólo el 50% tiene un vaso permeable hasta el pie ( generalmente la peronea). Existe una alta prevalencia de lesiones largas (mayores de 10 cm) y la afectación proximal suele ser escasa.
La elección de la técnica (bypass / angioplastia transluminal percutánea-PTA) va a depender del tipo de lesión y del riesgo quirúrgico que presente el paciente.
Las lesiones cortas (TASC A y B) presentan resultados buenos con el tratamiento endovascular, por lo este sería el tratamiento de primera elección. A medida que aumenta la longitud, la complejidad o la extensión de la enfermedad (TASC C y D), la revascularización abierta (bypass) consigue mejores resultados a largo plazo, por lo que la angioplastia sólo estaría indicada en pacientes con alto riesgo quirúrgico para la cirugía abierta.
La cirugía abierta (bypass fémoro-distal preferiblemente con vena safena), es una técnica compleja con una morbi-mortalidad asociada nada desdeñable (hasta el 18% en algunas series) aunque la permeablidad a largo plazo (5 años) es alta (60-80%) Por su parte las técnicas endovasculares son procedimientos menos agresivos, el éxito de la técnica dependerá de la longitud de la lesión y del número de vasos tratados. La permeabilidad a largo plazo es menor, sin embargo la tasa de salvamiento de la extremidad es similar a la de la cirugía. Teniendo en cuenta además, que el fallo de una angioplastia no impide la realización posterior de un bypass, cada vez son más los grupos que optan por las técnicas endovasculares como primera opción terapéutica en los casos de salvamiento de extremidad.
En general en pacientes con una esperanza de vida inferior a 2 años y una comorbilidad importante o en los que no hay vena útil, la angioplastia debe ser ofrecida como primera opción terapéutica; y en pacientes con expectativa de vida mayor a 2 años y buenas condiciones de vida, la cirugía ofrece mejores resultados a largo plazo con menor número de reintervenciones.
En aquellos pacientes con isquemia crítica sin opciones de revascularización, o con pies catastróficos , la amputación mayor es el tratamiento de elección
10.7.5 Descarga
Los dos componentes fundamentales de las úlceras en el pie diabético son la neuropatía y el aumento de la presión local. La reducción de la presión en el pie diabético es esencial para conseguir la cicatrización y evitar recidivas.
La descarga se puede hacer mediante férulas de contacto total, calzado modelado a medida, zapatos de apoyo posterior, plantillas, ortesis, cirugía (alargamiento del tendón de Aquiles, resección de las cabezas de los metatarsianos, osteotomías, exostectomías…), reposo en cama, silla de ruedas. Incluso técnicas tan sencillas como la eliminación de callosidades o el uso de fieltros de descarga plantar consiguen disminuir la presión de la zona.
Fig. 10 Férula de contacto
Es necesario que un profesional especializado (rehabilitador, podólogo, técnico ortopédico) realice una valoración del paciente y adapte las necesidades clínicas a las posibilidades técnicas, eligiendo el dispositivo que mejor se adapte a dichas necesidades y permita seguir realizando las curas.
10.7.6 Tratamiento de la neuropatía
La forma más efectiva para prevenir su aparición, como para mejorar la evolución de la neuropatía ya establecida es un estricto control glucémico (HbA1c < 6.5%).
Si el paciente presenta síntomas relevantes que interfieren con su calidad de vida (dolor, parestesias, disestesias, hiperestesias) se deben utilizar fármacos efectivos frente al dolor neuropático: antidepresivos tricíclicos (amitriptilina), anticonvulsivantes (gabapentina, pregabalina), inhibidores de la recaptación de serotonina y noradrenalina (duloxetina). Los opioides son eficaces aunque por sus efectos secundarios deben considerarse fármacos de segunda línea.
10.8 Neuroartropatía De Charcot
La artropatía de Charcot es la destrucción ósea y articular del pie con etiología no infecciosa, asociada a la neuropatía diabética; se caracteriza por dislocaciones articulares, fracturas patológicas y destrucción severa de la arquitectura del pie.
La etiología más ampliamente aceptada en el inicio del cuadro (artropatía de Charcot aguda) es el traumatismo (agudo o micro traumatismos de repetición) sobre un pie con neuropatía severa; como resultado de la neuropatía autonómica asociada y la apertura de shunt arterio-venosos, el flujo en el pie se incrementa provocando un aumento de la reabsorción ósea y dando lugar a osteopenia y debilidad ósea. La ausencia de sensibilidad protectora, impide al paciente percatarse tanto del traumatismo inicial como de la de la destrucción ósea que se va produciendo con la deambulación y continua caminado provocando un destrucción cada vez mayor.
El la fase aguda, el diagnóstico es clínico: importante edema del pie asociado eritema y aumento de temperatura sin presencia de lesiones y con neuropatía asociada. La radiografía puede ser normal o mostrar la presencia de fracturas patológicas y luxaciones articulares. Sin embargo el caso de que exista una lesión concomitante, el diagnóstico diferencial entre neuroartropatía y osteomielitis puede ser difícil, en estos casos la RMN, la gammagrafía, PET, cultivo óseo... pueden ser necesarios para establecer el diagnóstico.
Clásicamente se distinguen 3 etapas:
- Desarrollo y fragmentación: caracterizada por edema, destrucción ósea y luxación articular. Dura de 3 a 4 meses.
- Coalescencia: disminución del edema, formación de callos y consolidación de las fracturas.
- Consolidación: anquilosis e hipertrofia ósea, aparece deformidad, el pie queda ensanchado con prominencias óseas en la planta y en los bordes interno y externo.
Fig. 11 Neuroartropatía de Charcot
La etapa inicial es considerada activa, mientras que las dos últimas se consideran quiescentes o reparativas. El diagnóstico de la neuroartopatía en la fase inicial, en la que todavía no se ha producido ninguna deformidad, puede evitar la progresión de este proceso inflamatorio destructivo.
Las complicaciones de la neuropatía de Charcot incluyen ulceraciones en las áreas de prominencias óseas y amputaciones debidas a la infección/osteomielitis que se pueden desarrollar si se sobreinfectan dichas úlceras.
La clave del tratamiento en la fase aguda es el reposo y la inmovilización del pie, habitualmente mediante la colocación de férulas que se van cambiando cada 1-2 semanas, ajustándose al volumen del pie a medida que el edema disminuye. Cuando disminuye el edema y la temperatura del pie y aparece neoformación ósea en la radiografía (estado quiescente), se va permitiendo el apoyo progresivo, asistido con muletas u otros dispositivos de descarga. El tiempo medio hasta permitir el apoyo total varia entre 4 a 6 meses.
Una vez pasada la fase aguda, excepcionalmente, puede plantearse el tratamiento quirúrgico de las deformidades: exostectomías de protrusiones óseas a nivel plantar, medial o lateral; sección del tendón de Aquiles (en los casos de pie en mecedora, donde aumenta la carga en el medio pie); artrodesis … Si la deformidad es muy marcada o existe infección profunda puede ser necesaria la amputación
10.9 Unidades De Pie Diabético
Las unidades de pie diabético están formadas por un equipo multidisciplinario que proporciona una atención global a los problemas que pueden presentar los pacientes diabéticos en los pies, abarcando desde la prevención hasta el diagnostico y tratamiento. Está demostrado que con un enfoque multidisciplinar, se obtienen mejores resultados que con el abordaje tradicional, disminuyendo la mortalidad, la tasa de amputación y los costes.
Mediante la identificación y educación de los pacientes de riesgo, la detección precoz y el tratamiento adecuado de las complicaciones se puede disminuir la tasa de amputaciones en un 80% e incrementar la cicatrización de las úlceras en un 70-85%.
La conformación de este equipo puede variar en función de las características de cada área, pero debe incluir un cirujano vascular, un internista o especialista en enfermedades infecciosas, un endocrinólogo, un podólogo o personal de enfermería especializado en los cuidados de los pies (y que desempeñe además labores educativas y formativas sobre el cuidado de la diabetes y de los pies). Pueden incluir además un cirujano ortopédico, cardiólogo, nefrólogo, oftalmólogo…
Sus competencias deben incluir:
El cribado de todo diabético
- La identificación del pie de alto riesgo (deformidad, neuropatía, enfermedad arterial periférica, antecedentes de úlcera o amputación) con exámenes periódicos del mismo.
- Educación del paciente y su familia sobre la diabetes, cuidados de los pies, calzado apropiado y la necesidad de evaluación y tratamiento rápido de cualquier lesión en el pie.
- Control y tratamiento de la diabetes y de sus posibles complicaciones (factores de riesgo cardiovascular, insuficiencia renal, cardiopatía…)
- Valoración de las lesiones, proporcionando un tratamiento rápido y efectivo (curas, desbridamiento, descarga, valorar necesidad de antibioterapia, revascularización, cirugía ortopédica…)
10.10 Bibliografia
1. Blanes JI, Clara A, Lozano F et al. Consensus document on treatment of infections in diabetic foot. Rev Esp Quimioter. 2011 Dec;24(4):233-62
2. Frykberg RG, Zgonis T, Armstrong DG et al. Diabetic foot disorders. A clinical practice guideline (2006 revision). J Foot Ankle Surg. 2006 Sep-Oct;45(5 Suppl):S1-66.
3. Marinel.lo J, Blanes JI, Escudero JR, Ibañez V, Rguez-Olay JJ. Eds: Tratado de pie diabético. Jarpyo Editores. Madrid 2002:11-8
4. Benjamin A. Lipsky, Anthony R. Berendt, Paul B. Cornia et al. 2012 Infectious Diseases Society of America Clinical Practice Guideline for the Diagnosis and Treatment of Diabetic Foot Infections. Clin Infect Dis. (2012) 54 (12):e132-e173.
5. Grupo MBE Galicia. Neuropatía diabetica. Guías Clínicas 2006;6(18):1-4. Disponible en URL: http://www.fisterra.com. Abril 2009.
6. Schinca N, Álvarez J. Artropatía neuropática o Pie de Charcot. Biomedicina. 2012;7(1):44-50.
7. González de la Torre Héctor, Mosquera Fernández Abián, Quintana Lorenzo M.ª Luana, Perdomo Pérez Estrella, Quintana Montesdeoca M.ª del Pino. Clasificaciones de lesiones en pie diabético: Un problema no resuelto. Gerokomos [revista en la Internet]. 2012 Jun [citado 2015 Mayo 25] ; 23(2): 75-87
8. Canadian Diabetes Association Clinical Practice Guidelines Expert Committee, Booth G, Cheng AY. Canadian Diabetes Association 2013 clinical practice guidelines for the prevention andmanagement of diabetes in Canada. Can J Diabetes. 2013 Apr;37 Suppl 1:S4-7. doi: 10.1016/j.jcjd.2013.01.010. Epub 2013 Mar 26
9. Organización Mundial de la Salud. Diabetes. Nota descriptiva Nº 312. Disponible en URL: http://www.who.int/mediacentre/factsheets/fs312/es/ . Noviembre 2014
10. Boulton AJ, Vileikyte L, Ragnarson-Tennvall G, Apelqvist J. The global burden of diabetic foot disease. Lancet. 2005 Nov 12;366(9498):1719-24.
11. Norgren L, Hiat WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FGR, et al. Consenso inter-societario para el tratamiento de la enfermedad arterial periférica (TASC II). Eur J Vasc Endovasc Surg. 2007; 33:S1-S75.
12. Mark A. Creager, Joshua A. Beckman, Joseph Loscalzo. Medicina Vascular 2ª Edición 2014. Edit. Elservier Sanders
13. Rutherford´s Vascular Surgery. 8th Edition 2014. Edit. Elservier Sanders.
-