Capítulo 8 - Traumatismos Vasculares
8.1 Introducción
Los traumatismos constituyen la primera causa de muerte en las cuatro primeras décadas de la vida. El 80% de todos los accidentes lo sufren personas menores de 45 años. Los traumatismos vasculares representan el 3% de todos los traumatismos. El 80% de estas lesiones vasculares se producen en las extremidades, especialmente en las inferiores, tanto en la vida civil como en la militar y pueden comprometer la viabilidad de la extremidad. El 20% restantes son cervicales, torácicas o abdominales y pueden comprometer la vida del paciente.
Hasta la 2ª Guerra Mundial el tratamiento de las lesiones vasculares consistía fundamentalmente en la ligadura del vaso para cortar la hemorragia y esta intervención provoca una tasa de amputación del 50% de las extremidades tratadas. A pesar de que durante este conflicto se dieron algunos intentos de revascularización no es hasta la guerra de Corea, tras la introducción de pinzas vasculares atraumáticas, sutura monofilamento, prótesis sintéticas y la popularización de la arteriografía, que no se desarrolla el tratamiento moderno de los traumatismos vasculares, de forma que en esta guerra la tasa de amputaciones bajó hasta el 13%. El último avance importante se ha producido con la aplicación de técnicas endovasculares que han tenido gran impacto en el tratamiento de los traumatismos vasculares en la vida civil.
8.2 Mecanismos de Acción
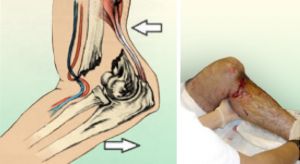
Los mecanismos de lesión se dividen en penetrantes y cerrados.
En los traumatismos penetrantes la lesión se produce por aplastamiento y separación de los tejidos a lo largo del trayecto del objeto penetrante, generalmente un objeto punzante o un proyectil. Estos objetos pueden producir la sección completa de una vaso (a veces se presenta con una hemorragia pero en otros casos se asocia trombosis del vaso), laceraciones parciales o disección de la pared del vaso.
En los traumatismos cerrados se producen las lesiones por compresión tisular o desaceleración brusca. En estos traumatismos se rompe la integridad de la estructura de la pared del vaso y las lesiones pueden ir desde un simple desgarro intimal o una mínima disección de la pared hasta una lesión transmural y trombosis.
La gravedad de una lesión depende de la energía cinética (EC) que se transfiere a los tejidos y que a su vez depende masa (M) y velocidad (V)
EC=MxV2/2
Los cambios de velocidad influyen en la transferencia de energía cinética mas que los cambios de masa.
Otro concepto a tener en cuenta en las lesiones vasculares es el fenómeno de la cavitación, que se produce cuando el tejido retrocede desde el punto de impacto con un objeto en movimiento alejándose del mismo.
Estos diferentes tipos de fuerzas causan deformidades, desgarros y rotura tisular.
En nuestro medio la yatrogenia supone el 38.3% de las causas de traumatismo vascular. Heridas por arma blanca y de fuego suman un 15%, mientras que el resto (45%) son accidente de causas múltiples: fracturas abiertas y cerradas, contusiones sin fractura, heridas por cristal y por asta de toro.
8.3 Tipos de Lesiones
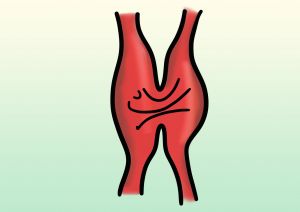
Las lesiones mas corrientes son las laceraciones parciales y las secciones completas. Las primeras suelen cursar con hemorragia persistente o formación de un seudoaneurisma, las segundas provocan una retracción de la íntima, trombosis de los extremos del vaso y signos de isquemia aguda.
Las formas de presentación mas frecuentes según el tipo de traumatismo pueden ser:
1.- Traumatismos penetrantes:
*Perforación lateral
* Sección completa
* Fístula arteriovenosa
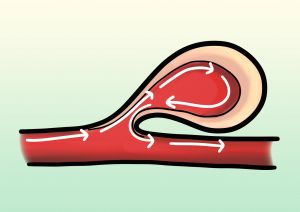
* Seudoaneurisma
2.- Traumatismos contusos
* Espasmo
* Contusión con fragmentación de la íntima en diversos grados de evolución.
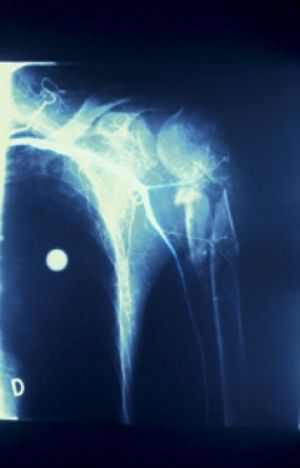
Fig. 1 Fractura subcapital de húmero con espasmode la arteria braquial
Fig. 2 Trombosis arterial
3.- Iatrogénicos:
* Trombosis (la más frecuente)
* Seudoaneurismas (sobre todo tras cateterismo cardiaco)
* Hemorragias
*Embolizaciónn distal
4.- Traumatismos en relación con toxicomanía :
* Puffy hand: obstrucción linfática y venosa superficialcrónica.
* Daño arterial directo (lesión intimal, trombosis,embolismo,falsos aneurismas y aneurismas micóticos).
* Complicaciones locales (celulitis, tromboflebitis, abscesos, …).
* Síndrome compartimental (por espasmo severo y posterior revascularización).
8.4 Clínica
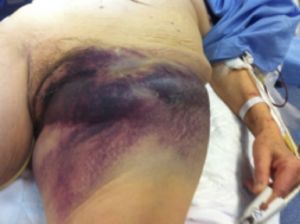
Las lesiones arteriales pueden producir cuatro tipos diferentes de manifestaciones clínicas: 1) hemorragia externa, 2) isquemia, 3) hematoma pulsátil y 4) hemorragia interna con signos de shock.
Sólo el 40% de los traumatismos vasculares se manifiestan primariamente con sintomatología propiamente isquémica, siendo los signos de sangrado los más frecuentes al inicio. Entre el 15 al 20% tienen una exploración completamente normal.
En general los síntomas en las lesiones arteriales se dividen en: duros (mayores) y blandos (menores).
Los signos duros o mayores corresponden a: ausencia de pulsos distales, hemorragia activa, isquemia aguda, hematoma pulsátil y soplo o frémito (thrill).
Los signos blandos o menores son la disminución de pulsos distales, lesión cercana al trayecto de un vaso importante, defecto neurológico, hipotensión arterial o shock.
En el tórax, la mayoría de las lesiones vasculares penetrantes se identifican en la cirugía al apreciarse hemotórax cuando se coloca un tubo torácico y, dependiendo de la pérdida de sangre, puede presentarse shock. Estos traumatismos penetrantes pueden asociarse también a lesiones en esófago, tráquea bronquios y corazón.
Toda herida penetrante en la caja torácica debe ser explorada quirúrgicamente porque cualquier retraso trae consecuencias devastadoras.
En cambio, en los traumatismos cerrados, la mayoría de las lesiones son arteriales y quedan contenidas por tejidos adyacentes, aunque el 80% de las personas que sufren un trauma vascular cerrado torácico mueren en el lugar del accidente, el resto son diagnosticados por presentar inestabilidad hemodinámica que no responde adecuadamente al fármacos o se detecta casualmente en las pruebas de imagen que se realizan en urgencias.
Las venas cava superior e inferior en su porción torácica rara se ven afectadas por traumatismos cerrados debido a su localización, baja presión y distensibilidad. Clínicamente se manifiestan con signos de taponamiento cardiaco. Las lesiones que se pueden presentar son penetrantes y exigen sutura vascular directa como tratamiento.
Las lesiones de las venas pulmonares son extremadamente raras, siempre penetrantes y se presentan con hemopericardio y taponamiento cardiaco
En el abdomen, las manifestaciones clínicas dependen de la presencia de taponamiento retroperitoneal. En estos casos el paciente puede estar hemodinámicamente estable o algo hipotenso, pero tiene mayores posibilidades de supervivencia. Cuando se pierde el taponamiento retroperitoneal se produce shock e hipovolemia aguda. Las lesiones contusas de las arterias viscerales son muy poco frecuentes y las lesiones penetrantes cursan con hemoperitoneo y shock.
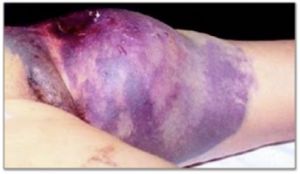
En las extremidades el signo mas frecuente en las lesiones vasculares es la isquemia aguda: heridas punzantes, proyectiles a baja velocidad y traumatismos contusos asociados a luxaciones y fracturas. La hemorragia externa es menos frecuente y se observa en traumatismos por armas de fuego de alta velocidad.
Fig. 3 Hematoma pulsátil post cateterismo
8.5 Diagnóstico
Una correcta exploración física nos orientará sobre la existencia o no de lesiones vasculares: el estado general del paciente, el grado de estabilidad hemodinámica, la localización de orificios de entrada, la presencia de posibles lesiones óseas o articulares, la existencia de hemorragia o de signos de isquemia, la presencia o ausencia de pulsos, la coloración y temperatura de la extremidades, los déficit neurológicos motores o sensitivos, lapresencia de tumoraciones pulsátiles o no en la proximidad de la lesión, soplos o frémitos deben ser explorados y evaluados.
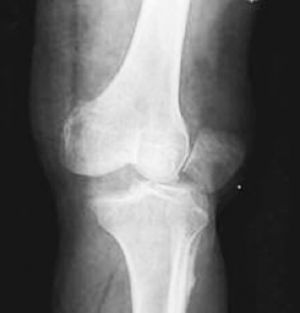
Fig. 4 Luxación de rodilla
En la mayoría de casos la sospecha clínica debe ser confirmada con otras pruebas diagnósticas tanto para detectar lesiones ocultas como para establecer una estrategia quirúrgica adecuada. Las principales herramientas son:
8.5.1 xploraciones vasculares no invasivas
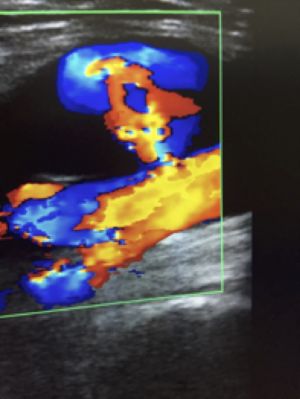
El eco-doppler está indicado para descartar daño arterial oculto o bien para confirmar la permeabilidad del árbol arterial en un paciente que suele ser difícilmente explorable por edema importante o por lesiones asociadas (fracturas abiertas). Es de gran utilidad el índice Tobillo/Brazo para evaluar posibles oclusiones arteriales.
Fig. 5Seudoaneurisma. Eco-doppler
8.5.2 Rx Simple
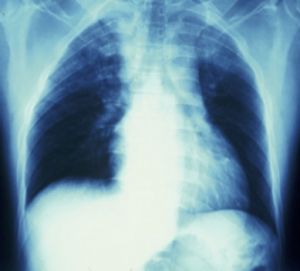
La Rxsimple de tórax o de las extremidades puede orientarnos sobre la presencia de posibles lesiones vasculares. Ensanchamiento mediastínico puede ser secundario a rotura de aorta torácica y fracturas o luxaciones asociados a signos de isquemia pueden hacer sospechar la existencia de trombosis por traumatismo de tipo contuso.
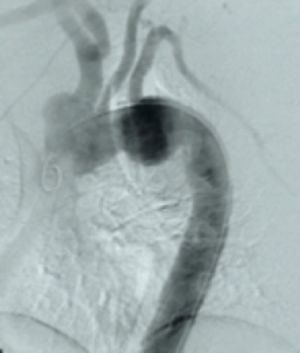
Fig. 6 Ensanchamiento mediastínico
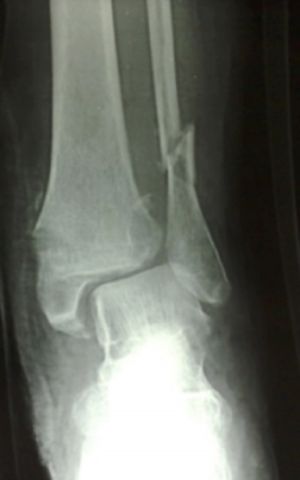
Fig. 7 Fractura luxación de tobillo
8.5.3 AngioTAC/AngioRNM
Tanto el angioTAC como la AngioRNM han demostrado gran utilidad para el diagnóstico precoz de lesiones vasculares traumáticas siendo especialmente útiles en las lesiones cervicales, torácicas y abdominales. En las extremidades, especialmente en vasos distales, no tienen suficiente definición,y es preferible la arteriografía. Hoy día la disponibilidad y rapidez de los estudio TAC hace que se utilice como primera prueba diagnóstica para despistaje de lesiones vasculares.
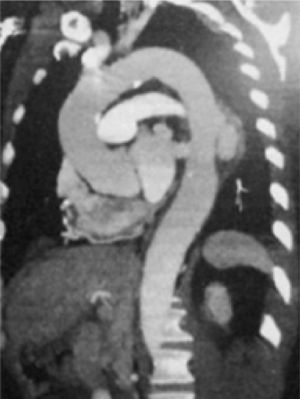
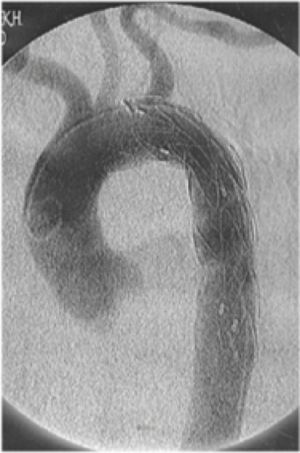
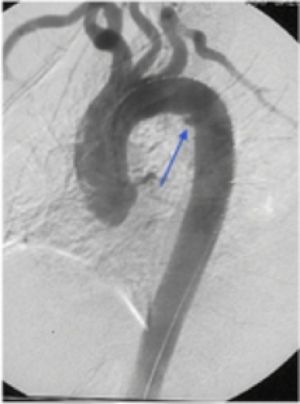
Fig. 8 Rotura aorta descendente
8.5.4 Arteriografía
Sigue siendo la piedra angular del diagnóstico en traumatismos vasculares y permite:
1.- Determinar localización y extensión precisa, con la posibilidad de afectación de varios vasos.
2.- Diagnosticar el daño vascular cuando la presentación clínica es equívoca, con miras a evitar cirugías innecesarias.
3.- Como acceso y control de vasos dañados (por ejemplo embolización).
Indicaciones de la arteriografía:
- Heridas asociadas a fractura y traumatismo contuso.
- Heridas por arma de fuego.
- Heridas en pacientes con vasculopatía periférica previa.
- Sospecha de falso aneurisma y/o fístula arteriovenosa.
- Cuando el índice T/B < 1.
- Déficit neurológico.
La única contraindicación absoluta es el antecedente de reacción anafiláctica al contraste, mientras que el bajo gasto cardiaco, la anuria, infecciones locales, hemorragia, alergias al contraste y diabetes mellitus con insuficiencia renal son contraindicaciones relativas.
Vías de acceso:
1.- Transfemoral.
2.- Braquial / axilar derecha
Hallazgos arteriográficos:
* Stop de contraste.
* Irregularidad del contorno del vaso.
* Defectos de relleno.
* Relleno venoso prematuro=fístula arteriovenosa.
* Extravasación de contraste, relleno de un falso aneurisma.
El papel de la angiografía puede ser fundamental en el traumatismo vascular, sobre todo en las fracturas pélvicas, para el mejor control de la exsanguinación. El sangrado pélvico arterial suele ser difuso, por lo que es mal controlado mediante la ligadura quirúrgica, siendo mejor manejado mediante embolización percutánea por catéter.
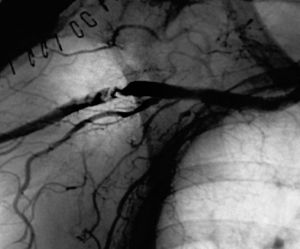
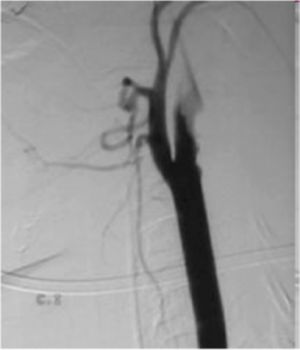
Fig. 9 Contusión arteria axilar
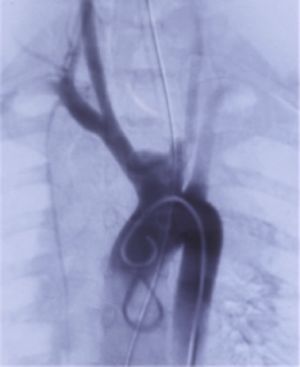
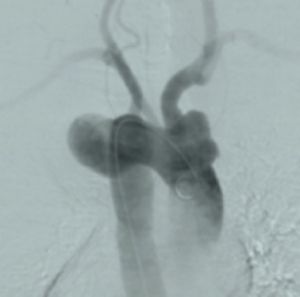
Fig. 10 Rotura arco aórtico
8.6 Tratamiento
El tratamiento de las lesiones arteriales de pequeño tamaño, no oclusivas, asintomáticas, detectadas angiográficamente es motivo de controversia y algunos equipos son partidarios de seguimiento evolutivo sin tratamiento quirúrgico mientras que otros grupos son partidarios de intervenir todas las lesiones.
El tratamiento endovascular mediante embolización (traumatismos pélvicos, fístulas arterio-venosas de bajo flujo o arterias de difícil acceso) o la inyección de trombina en seudoaneurismas (post cateterismos) tienen amplia aceptación aunque no siempre son resolutivos. Otra técnica endovascular consiste en el uso de endoprótesis que permiten mantener la luz del vaso abierta y evita la hemorragia. Hoy día son ampliamente utilizados en la roturas de aorta torácica o en lesiones de los grandes vasos supraaórticos o en pacientes de alto riesgo con lesiones concomitante en extremidades.
Fig. 11 Endoprótesis en aorta descendente
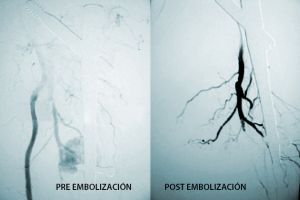
Fig. 12 Pseudoaneurisma femoral profunda yatrogénico tratado mediante embolización
Para los pacientes que precisan abordaje quirúrgico abierto existen numerosas técnicas de reconstrucción vascular: suturavascular directa, trombectomía y plastia vascular,by-pass con vena o prótesis e incluso la simple ligadura del vaso. Estas intervenciones tienen mayor tasa de fracaso en los traumatismos contusos que en los abiertos, especialmente en las extremidades.
El organigrama de actuación terapéutica general debe de seguir el siguiente orden :
A.- Preparación para la cirugía:
• Estabilización hemodinámica y de vías respiratorias. Hay que mantener al menos 2 vías venosas periféricas de grueso calibre para administración de sangre y sueros si precisa.
• Heparina: beneficiosa en pacientes con isquemia prolongada secundaria a lesiones vasculares aisladas. No debe darse en pacientes con lesiones asociadas del sistema nervioso central, oftalmológicas, torácicas, o del sistema músculo esquelético.
• Antibioterapia: efectiva contra gérmenes Gram positivos (colonizadores de la piel ) como el estafilococo. Es suficiente con un tratamiento de menos de 48 horas.
B.- Actuación local sobre la zona traumatizada:
1.- Desbridamiento:
Su propósito es el volver una herida infectada en otra contaminada y con tejidos sanos para que pueda seguir el proceso normal de cicatrización. Si no se realiza de forma adecuada la herida podrá infectarse complicando cualquier otro procedimiento quirúrgico.
El desbridamiento puede efectuarse de dos formas: por un lado la irrigación/lavado y por otro con el desbridamiento quirúrgico. En el primer caso se efectúa un arrastre mecánico de los gérmenes y materiales extraños. Esto se puede realizar de forma satisfactoria con suero salino fisiológico estéril sobre la herida, sin descuidar la irrigación bajo los colgajos cutáneos y recovecos de la herida. No está claro si el empleo de antibióticos tópicos en el líquido de irrigación supone alguna ventaja adicional, por ello no se emplean de forma sistemática. La irrigación es más efectiva si se realiza de forma intermitente o pulsátil a baja presión.
El desbridamiento quirúrgico consiste en remover todos los tejidos devascularizados e inviables, conservando los sanos, la mejor forma de determinar esto es mediante el sangrado activo de los tejidos. La escisión de los bordes de la herida que se realiza de forma casi sistemática, no es siempre necesaria, salvo que haya dudas en la viabilidad de los mismos. Siempre que haya dudas en la viabilidad de un tejido es importante tener en cuenta el concepto de “second look o segundo vistazo” de los autores anglosajones, que consiste en una segunda inspección 2-3 días más tarde para comprobar el estado de los tejidos y si es necesario completar el desbridamiento inicial, puede realizarse también revisiones posteriores si el estado de la herida así lo recomienda.
Deben explorarse los tejidos de forma detallada y por planos, los tejidos devascularizados deben resecarse pues su destino es la necrosis, los amplios despegamientos cutáneos suponen la rotura de las perforantes cutáneas y el riesgo de necrosis de los tejidos.
2.- Estabilización de las fracturas:
Debe de lograrse una estabilización y reducción adecuada de las fracturas, cualquier método debe de perseguir una osteosíntesis sólida que permita la movilidad precoz y minimice las rigideces articulares. Se realiza de forma precoz pues así se evita el edema, la formación de cicatrices y fibrosis. En presencia de fracturas muy conminutas es preferible ser conservador retirando sólo los fragmentos muy pequeños, cuando existe una pérdida ósea importante se precisa de un injerto óseo, con una herida limpia y una cobertura adecuada puede realizarse el injerto óseo de urgencia, sino es preferible posponer el injerto a un segundo tiempo, hasta entonces se mantendrá la arquitectura y longitud ósea habitualmente con el empleo de agujas de Kirchner acodadas o mediante fijadores externos.
3.- Revascularización:
La revascularización supone la reparación de los ejes vasculares lesionados, con ello se evita necrosis tisulares, aumenta su resistencia a la infección, favorece la consolidación ósea, la regeneración nerviosa y la curación de cualquier tejido.Cuando hay algún segmento del miembro devascularizado es obvio que se debe proceder a la reparación vascular, aún en presencia de una isquemia compensada debe plantearse su reparación, pues pueden aparecer signos de déficit vascular posteriormente. Cuanto más proximal sea la lesión vascular mayor será la posibilidad de isquemia muscular y por tanto la urgencia de la reparación. El resultado final tras una lesión y todas las reparaciones que se hallan realizado dependen del aporte sanguíneo de esa extremidad, por ello debe ser la prioridad máxima en el tratamiento de las lesiones vasculares de las extremidades, y sólo el riesgo vital del paciente se encuentra por encima de esta prioridad.
C.- Reparación de las estructuras profundas:
Las lesiones tendinosas sin pérdidas de sustancia pueden ser reparadas de forma primaria, mientras que si existe una pérdida de sustancia tendinosa importante es preferible una reparación secundaria mediante injertos tendinosos, en el caso de los tendones flexores si la calidad de cobertura cutánea es adecuada puede iniciarse el proceso de reconstrucción tendinosa de urgencia.
Las lesiones nerviosas limpias sin pérdidas de sustancia deben ser reparadas de forma primaria pues se obtienen resultados mejores que con una reparación secundaria, por el contrario en presencia de una lesión contusa del nervio con pérdida de sustancia y una herida sucia es preferible su reparación secundaria mediante injertos cuando la situación local lo permita.
El examen muscular debe ser minucioso, las masas musculares desvitalizadas deben de ser resecadas de forma amplia por el riesgo de complicaciones sépticas por anaerobios, además los músculos isquémicos se vuelven tejido fibroso originando retracciones y rigideces articulares complicando las cirugías secundarias.
D.- Cobertura cutánea:
Existe un amplio abanico de posibilidades para lograr el cierre de una herida: desde el cierre directo hasta el empleo de colgajos deben ser evaluados por el cirujano que deberá optar por la manera más segura y apropiada de reparación de la herida.
En conclusión, los problemas vasculares de una extremidad pueden ser primarios, por lesión arterial y una isquemia por falta de aporte, o secundarios por problemas de retorno venoso, ya que pueden producir edema y un aumento de presión en un compartimento que agrave la obstrucción venosa, se crea así un círculo vicioso en el que el resultado final será la obstrucción al flujo arterial.Aunque la reparación venosa es requerida con mucha menor frecuencia es habitual el realizar la apertura de los estuches aponeuróticos cerrados para evitar la aparición de un síndrome compartimetal secundario.
La pauta a seguir debería ser:
Estabilización de fracturas óseas: Hay que realizar siempre primero la reconstrucción traumatológica para evitar tracciones bruscas tras la reparación arterial. Solo deberá realizarse la cirugía arterial antes que la estabilización ósea si existe isquemia importante que ponga en peligro la extremidad.
Reconstrucción venosa: precede a la arterial si la vena lesionada es la mayor o única fuente de retorno venoso ( mejora el out-flow y por lo tanto el éxito de la reparación arterial ) .
Reconstrucción arterial y restablecimiento del flujo: se pueden realizar diversas técnica, las mas habituales son
1- Sutura simple.
2.- Plastia venosa/prótesis tras trombectomía.
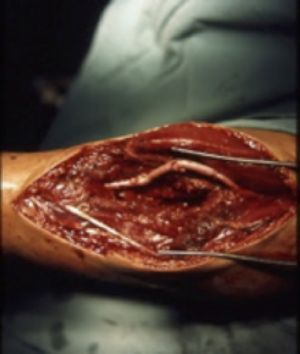
3.- By-pass con vena autóloga (safena o cefálica ), obtenida del miembro contralateral para preservar el flujo venoso superficial del miembro dañado o con by-pass con prótesis de PTFE en caso de imposibilidad de obtener vena. La vena parece el material más resistente a la infección, debiéndose recubrir con músculo viable.
Fig. 13 By-pass con vena
4.- En algunos casos la ligadura del vaso, especialmente en venas o arterias tibiales o del antebrazo puede ser una opción terapéutica.
Fasciotomía precoz : se debe plantear dependiendo del tiempo y severidad de la isquemia.
Amputación directa: en isquemias muy evolucionadas, y en asociación de daño arterial, neurológico y pérdida importante de partes blandas. Nunca el daño vascular por si mismo decide la amputación.
8.7 Características de los Traumatismos según Topografía
8.7.1 Traumatismos vasculares cervicales
Las estructuras cervicales que más se lesionan en los traumatismos son los vasos sanguíneos y suponen hasta el 20% en las lesiones penetrantes, en cambio en los traumatismos cerrados es rara su lesión. Se presentan relacionados con accidentes de coche (82%), accidentes de moto (7%) y agresiones (6%).
Suelen ser varones, jóvenes y sanos en
los que el consumo de alcohol o drogas es el desencadenante de la lesión.
Fig. 14 Zonas cervicales
El vaso que más se lesiona es la carótida común, por encima incluso de la interna.
La localización de las lesiones se divide en tres zonas:
Zona I: desde la escotadura yugular hasta cricoides.
Zona II: desde cricoides hasta el ángulo de la mandíbula.
Zona III: desde ángulo de la mandíbula hasta la base del cráneo.
Si solo hay signos clínicos menores (blandos) no se aconseja la exploración quirúrgica inmediata sin otras pruebas diagnósticas que confirmen la existencia de una lesión vascular. Si la lesión penetrante es profunda o hay signos clínicos mayores (duros) las pruebas diagnósticas y la intervención quirúrgica deben ser inmediatas. La prueba diagnóstica vascular de elección es la angiografía pero los angioTAC actuales aportan gran calidad de imagen, precisión y nos informan de lesiones asociadas en otras
estructuras anatómicas.
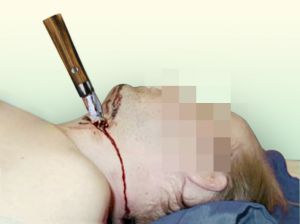
Fig. 15 Traumatismo penetrante cervical por arma blanca
Otras pruebas como lanringoscopia, broncoscopia o esofagoscopia pueden ser necesarias para valorar estas estructuras y detectar lesiones ocultas.
Las lesiones en las zonas I y II suele ser subsidiarias de tratamiento quirúrgico y las de la zona III de tratamiento endovascular mediante embolización o prótesis endovasculares. El abordaje quirúrgico de la zona I es complejo y suele precisar la realización de esternotomía para un adecuado control de la salida de los troncos supraaórticos, en cambio el abordaje de los vasos incluidos en la zona II suele ser fácil a través de una incisión a los largo del borde interno del músculo esternocleidomastoideo. El abordaje de los vasos de la zona III es difícil y exige una extensa exposición cefálica, a veces asociada a luxación o sección mandibular. En los últimos años, el desarrollo de técnicas endovasculares como embolizaciones y endoprótesis ha permitido, sobre todo en lesiones de las zonas I y III, minimizar las complicaciones secundarias al abordaje quirúrgico y la yatrogenia; sin embargo su uso está limitado por la anatomía de los vasos y el riesgo de embolizaciones cerebrales, hiperplasias intimases y reestenosis.
En casos de sospecha de lesiones cerradas en arterias carótidas o vertebrales, aunque poco frecuentes, se debe actuar de forma inmediata ya que provocan isquemia cerebral en el 40-80% de los pacientes y una mortalidad que oscila entre 25 y 60%. Estas lesiones pueden asociarse a fracturas de la base del cráneo, macizo facial medio, vértebras cervicales o mandíbula, tracción o torsiones cervicales bruscas casos de estrangulación.
El angioTAC es una prueba rápida y con alta sensibilidad (94%), pero la angiografía digital siendo el estudio de referencia, especialmente en los traumatismos cerrados.
Fig. 16 Disección carótida interna post traumatismo cervical
La escala de Denver es el método comúnmente aceptado de clasificación de las lesiones encontradas en el TAC o la angiografía:
En las lesiones I, II y IV la anticoagulación es la base del tratamiento ya que los datos acumulados indican que se evita el infarto cerebral en la mayoría de los casos y no hay diferencia comparando los pacientes tratados con cirugía abierta o endovascular, mientras que en las III y V es mas adecuado tratarlas mediante procedimiento quirúrgico, ya sea abierto o endovascular.
En las lesiones venosas cervicales puede ligarse el vaso si la lesión es unilateral pero en las venas y lesiones bilaterales es preferible la reconstrucción vascular.
8.7.2 Traumatismos aorta torácica
La mayoría de los traumatismos con sección aórtica producen una exsanguinación brusca y muerte inmediata del paciente (80-90%), de los que llegan al hospital el 38% morirán por las lesiones asociadas de otros órganos, la mayoría en las primeras 24 horas.
Las lesiones contusas en aorta torácica se deben a desaceleración brusca, principalmente relacionados con colisiones frontales y laterales en accidentes de tráfico o precipitados. La mayoría son distales al origen de la arteria subclavia izquierda (65%), cayado (10%), aorta descendente (12%) y múltiples lesiones (13%).
Las lesiones penetrantes por heridas punzantes se presentan generalmente en aorta ascendente mientras que las de aorta descendente corresponden a heridas por armas de fuego.
Fig. 17 Laceración aorta torácica
Fig. 18 Sección completa aorta
Fig. 19 Rotura a nivel del arco
La reparación quirúrgica abierta se realiza a través de toracotomía izquierda a la altura del 4º espacio intercostal, se controla la aorta proximal y distal a la zona traumatizada y se repara la lesión mediante sutura directa o por interposición de una prótesis. Hoy día no es la opción ideal ya que puede empeorar las lesiones asociadas en otros órganos (contusión pulmonar, contusión cardíaca) y se asocia a un alto porcentaje de lesiones medulares.
Actualmente el tratamiento de elección es endovascular y debe realizarse en centros dotados de equipos de angiorradiología digital. Se realiza bajo anestesia general, por vía transfemoral y con el paciente hipotenso.
8.7.3 Traumatismos vasculares abdominales
Son frecuentes en la vida civil y pueden llegar a representar hasta el 30% de todas las lesiones vasculares. En un 90-95% de los casos son penetrantes. Los vasos que mas se lesionan son la aorta (25%) y la vena cava inferior (33%). La mortalidad hospitalaria oscila entre el 30 y el 80% en las lesiones de aorta abdominal y 65% en las de vena cava inferior. La muerte es por hemorragia.
En el 90% de los casos se presenta un hematoma retroperitoneal y shock. Salvo en casos de hematoma retroperitoneal pélvico, que puede ser tratado de forma conservadora o endovascular, el resto de los traumatismos vasculares abdominales precisa una exploración quirúrgica urgente. En los pacientes hemodinámicamente estables puede realizarse estudios de imagen para confirmar la sospecha diagnóstica y localizar el vaso lesionado. La ecografía puede ser un método útil pero en estos casos el TAC es la prueba por excelencia. la angiografía es de mayor utilidad para el tratamiento endovascular.
8.7.4 Traumatismos en arterias subclavia y axilar
Gracias a que el trayecto de los vasos subclavio y axilar está protegido por la clavícula y el músculo pectoral no son traumatismos vasculares frecuentes. La mayoría de las lesiones de estas arterias se deben a traumatismos penetrantes, los traumatismos contusos son poco frecuentes y se asocian generalmente a fractura o luxación de clavícula y primera costilla. En un 20% de los casos de traumasubclavio/axilar se produce una lesión de la arteria y la vena. Tienen una alta mortalidad (39%) y en muchos casos los pacientes no llegan vivos al hospital.
<
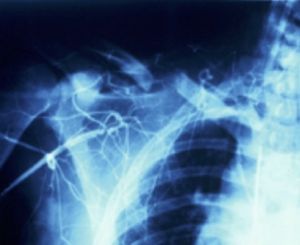
Fig. 20 Trauma contuso a. subclavia por fractura clavícula
En los pacientes hemodinámicamente inestables, con hemorragia activa o con isquemia de la extremidad superior no debe retrasarse la intervención, en aquello es situación de estabilidad conviene la realización de estudios diagnósticos para valorar la localización exacta de la lesión.
El abordaje quirúrgico abierto obliga a una amplia incisión desde la escotadura yugular, pasando por encima de clavícula y finalizando en el surco pectoral.
El tratamiento endovascular ha demostrado ser especialmente útil en pacientes estables y que presentan seudoaneurismas, fístulas arteriovenosas traumáticas y disecciones locales.
8.7.5 Traumatismos vasculares en extremidades
Suponen el 70-80% de los traumatismos vasculares y afectan sobre todo a varones entre 20 y 40 años, son más frecuentes las lesiones penetrantes que las contusas (10:1). Las arterias que se lesionan con mayor frecuencia son braquial, femoral y poplítea, aunque en esta última la mayoría de sus lesiones corresponden a traumatismos contusos.
El diagnóstico mediante eco-doppler es útil por su precisión, rapidez y bajo coste pero está limitada a la hora de detectar pequeños defectos de la pared vascular. El índice tobillo/brazo nos orientará sobre la repercusión del flujo arterial distal a la lesión. El angioTAC y angioRNM son estudios mas caros pero que ofrecen mejor resolución anatómica de las lesiones.
La angiografía además de permitirnos evaluar las lesiones nos posibilita realizar tratamientos endovasculares.
Los traumatismos arteriales en la extremidad superior suponen el 30% del total de los traumatismos vasculares, el mecanismo es casi siempre penetrante y en un 50% de los casos la lesión se localiza en la arteria humeral (braquial). Se asocia a la lesión ósea, nerviosa o venosa hasta en un 70% de los casos. La funcionalidad va a depender de la lesión nerviosa y son traumatismos con escasa mortalidad.
Aunque clínicamente debutan con hemorragia externa, la isquemia crítica puede aparecer a las 4 horas de la lesión por lo que la reconstrucción vascular debe ser inmediata. Se ha comprobado que si la revascularización se retrasa 12 horas desde el traumatismo solo el 25% de los pacientes recupera la funcionalidad completa de la extremidad.
Los traumatismos de los vasos femoralessuponen el 70% de los traumatismos vasculares en las extremidades. El 90% de estos traumatismos son penetrantes y la mayoría por herida de bala. La hemorragia es el signo clínico mas frecuente.
El tratamiento quirúrgico abierto con reconstrucción de la continuidad arterial ha disminuido la tasa de amputación al 9%.
En este sector, cuando la lesión afecta a arteria y vena, es preferible la reconstrucción de la vena lesionada antes que la ligadura simple ya que las secuelas del síndrome post-trombótico secundario puede limitar mucho la calidad de vida del paciente.
La arteria poplítea es la segunda arteria del miembro inferior en porcentaje de traumatismos. La lesión cerrada se asocia a fracturas y luxaciones de rodilla.
Fig. 21 Luxación de rodilla
Entre 20 y 38% se asocia a lesiones venosas o nerviosas. El daño sufrido por estas estructuras, los huesos y la musculatura desempeña un papel importante en el rescate de la extremidad y actualmente las estadísticas mas favorables contemplan un 11% de amputaciones cuando se valora el conjunto de todos los traumatismos poplíteos y un 54% cuando hay lesiones óseas, nerviosas o de partes blandas asociadas.
El tratamiento de elección suele precisar la realización de by-pass con vena mediante cirugía abierta.
Fig. 22 Traumatismo en pierna tratado mediante by-pass con vena
8.8 Traumatismos Vasculares Yatrógenos
El aumento de lesiones vasculares yatrógenas se asocia al aumento de procedimientos diagnósticos y terapéuticos realizados con catéter percutáneo para tratar enfermedades cardiovasculares (cateterismos).
La mayoría de estas lesiones deben, por tanto, ser consideradas penetrantes. En nuestra experiencia supone el 40% de todos los traumatismos vasculares aunque con una mortalidad 4 veces menor que el resto de los traumatismos.
En algunos casos pueden ser reparadas por procedimientos endovasculares pero la mayoría precisa intervención quirúrgica, aunque depende de la situación hemodinámica del paciente y del grado de isquemia que presente.
Las lesiones mas frecuentes son: seudoaneurismas y fístulas arteriovenosas.
El seudoaneurisma es un hematoma encapsulado que se produce en una arteria punzada tras sellado incompleto a nivel de la capa media de dicho vaso (disrupción de la pared arterial). Dada la inadecuada hemostasia, y la continua extravasación sanguínea dentro del tejido subcutáneo a través del orificio de punción, el hematoma es contenido dentro de una pseudocápsula de tejido fibroso, en el tejido subyacente a la punción. Su incidencia varía entre el 0,05 al 4%, pero en raras ocasiones puede llegar al 11-16% en pacientes anticoagulados.
La sospecha de un seudoaneurisma se produce por dolor, hematoma superficial o la aparición de una tumoración tumefacta y pulsátil en zona de punción del cateterismo, habitualmente en región inguinal.
A la exploración podemos encontrar hemorragia pulsátil activa, tumoración pulsátil y soplo a la auscultación.
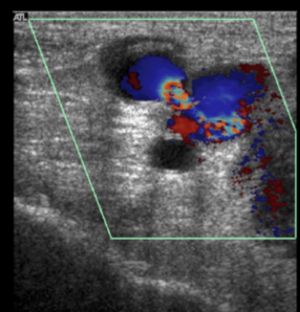
Fig. 23 Seudoaneurisma femoral post cateterismo
El método diagnóstico de elección es el eco-doppler que tiene un presión diagnóstica casi del 100%, pero en pacientes muy obesos o en grandes hematomas puede ser útil el TAC para precisar el diagnóstico.
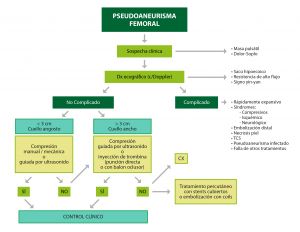
Muchos de estos casos pueden tratarse de forma conservadora. Los pacientes con seudoaneurismas que no producen dolor intenso, tienen < 3cm de diámetro y no precisan estar anticoagulados se obstruyen espontáneamente en un 80-90% de los casos en el primer mes. Si el paciente amenaza de necrosis cutánea,presenta dolor intenso (compresión del nervio femoral), hemorragia activa a pesar de la compresión o tiene signos de isquemia distal el paciente debe ser intervenido quirúrgicamente de forma urgente.
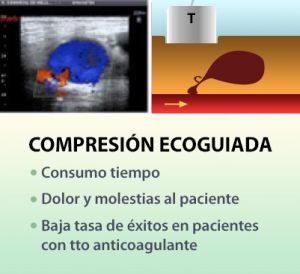
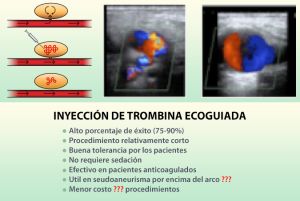
En casos de pacientes estables pueden intentarse varias formas de acelerar la oclusión del seudoaneurisma: mediante compresión ecoguiada del orificio de entrada del flujo arterial al seudoaneurisma durante un periodo de 30-40 minutos hasta comprobar que se ha trombosado o mediante la inyección de trombina bajo control ecográfico en el seno del seudoaneurisma ( se pincha con una aguja del 22 y se administra hasta 1000 UI de trombina humana) y se controla hasta la desaparición del flujo en su interior. Se han descrito hasta un 9% de recidivas con este procedimiento y 2% de riesgo de trombosis arterial o embolización distal.
Fig. 24 Compresión ecoguiada
Fig. 25 Inyección de trombina ecoguiada
La reparación endovascular ha dado buenos resultados en vasos viscerales pero en la ingle, a pesar de su fácil colocación, pueden dar problemas a corto plazo ya que se trata de una zona de flexión que puede provocar rotura y trombosis de la endoprótesis.
La reparación quirúrgica se debe realizar si la compresión ecoguiada y la inyección de trombina fracasan y existe amenaza de necrosis cutánea,el dolor es intenso, hemorragia activa o tiene signos de isquemia distal. Habitualmente se aborda directamente la femoral común, aunque hay casos en que es preciso un control retroperitoneal del vaso, se controla la arteria, se buscan todos los posibles orificios hemorrágicos y se reparan con sutura monofilamento.
Las fístulas arteriovenosas traumáticas pueden ser clínicamente menos expresivas que otras complicaciones y se caracterizan por la presencia de un soplo a nivel de la zona de punción. La intensidad del soplo se correlaciona directamente con la intensidad de la fístula. Con el tiempo las
fístulas tienden a aumentar aunque no suelen llegar a desarrollarse tanto como las fístulas construidas para hemodiálisis.
La sospecha diagnóstica puede confirmarse mediante eco-doppler: flujo turbulento a nivel de la fístula, aumento del flujo venoso proximal en la vena femoral, no se detectan cambios en el flujo venoso con la maniobra de Valsalva y disminución del flujo arterial distal a la fístula.
Fig. 26 Fístula AV. Eco-doppler
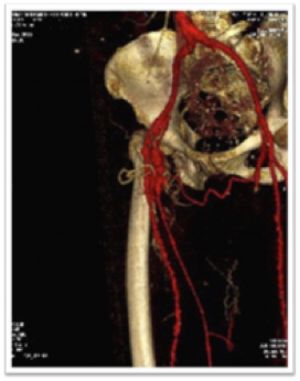
Fig. 27 AngioTAC de FAV arteriovenosa post cateterismo
El TAC no suele ser de gran utilidad en estos casos.
El tratamiento endovascular en esta zona no es útil a medio plazo y el tratamiento quirúrgico es complejo dada la friabilidad de los vasos y riesgo de hemorragia. Técnicamente hay que suturar la fístula y restablecer el flujo normal.
8.9 Bibliografía
1. Medicina Vascular. Complemento de Braunwald. Tratado de Cardiología. 2ª Edición. Mark A. Greager, Joshua A. Beckman. Edt Elservier Saunders 2013.
2. Cirugía Vascular. Sexta Edición. Rutherford. Elservier Saunders 2006
3. Girma Tefera. Traumatic thoracic aortic injury and ruptures. J Vasc Surg 2010, 52: 41S-44S
4. Nguyen T, Kalish J, Woodson J. management of civilian and military Vascular Trauma: Lessons learned. Seminars in Vascular Surgery 23: 235-242. 2011
5. Richens D, Kotidis K, Neale M, Oakley C, Fails A. Rupture of the aorta following road traffic accidents in the United Kingdom 1992–1999. The results of the cooperative crash injury study. Eur J Cardiothorac Surg 2003;23:143–148.
6. Neschis DG, Scalea TM, Flinn WR,Griffith BP. Blunt aortic injury.NEngl J Med2008; 359:1708–1716.
7. Azizzadeh A, Keyhani K, Miller CC 3rd, Coogan SM, Safi HJ, Estrera AL. Blunt traumatic aortic injury: initial experience with endovascular repair. J Vasc Surg 2009;49:1403–1408.
Mosquera VX, Marini M, Muniz J, Asorey-Veiga V, Adrio-Nazar B, Boix R, Lopez-Perez JM, Pradas-Montilla G, Cuenca JJ. Traumatic aortic injury score (TRAINS): an easy and simple score for early detection of traumatic aortic injuries in major trauma patients with associated blunt chest trauma. Intensive Care Med 2012;38:1487–1496.
8. Smith MD, Cassidy JM, Souther S, Morris EJ, Sapin PM, Johnson SB, Kearne PA. Transesophageal echocardiography in the diagnosis of traumatic rupture of the aorta. N Engl J Med 1995;332:356–362.
9. Vignon P, Gueret P, Vedrinne JM, Lagrange P, Cornu E, Abrieu O, Gastinne H, Bensaid J, Lang RM. Role of transesophageal echocardiography in the diagnosis and management of traumatic aortic disruption. Circulation 1995;92:2959–2968.
10. Murad MH, Rizvi AZ, Malgor R, Carey J, Alkatib AA, Erwin PJ, LeeWA, Fairman RM. Comparative effectiveness of the treatments for thoracic aortic transection [corrected]. J Vasc Surg 2011;53:p193–199 e1–e21.
11. Malhotra AK, Fabian TC, Croce MA, Weiman DS, Gavant ML, Pate JW. Minimal aortic injury: a lesion associated with advancing diagnostic techniques. J Trauma 2001;51:1042–1048.
12. Lee WA, Matsumura JS, Mitchell RS, Farber MA, Greenberg RK, Azizzadeh A, Murad MH, Fairman RM. Endovascular repair of traumatic thoracic aortic injury: clinical practice guidelines of the Society for Vascular Surgery. J Vasc Surg 2011;53:187–192.
13. Fabian TC, Davis KA, Gavant ML, Croce MA, Melton SM, Patton JH Jr., Haan CK, Weiman DS, PateJW. Prospective study of blunt aortic injury: helicalCTis diagnostic and antihypertensive therapy reduces rupture. Ann Surg 1998;227:p666–676; discussion 676–677.
14. Fabian TC, Richardson JD, Croce MA, Smith JS Jr, Rodman G Jr, Kearney PA, Flynn W, Ney AL, Cone JB, Luchette FA, Wisner DH, Scholten DJ, Beaver BL, Conn AK, Coscia R, Hoyt DB, Morris JA Jr, Harviel JD, Peitzman AB, Bynoe RP, Diamond DL, Wall M, Gates JD, Asensio JA, McCarthy MC, Girotti MJ, VanWijngaarden M, Cogbill TH, Levison MA, Aprahamian C, Sutton JE Jr., Allen CF, Hirsch EF, Nagy K, Bachulis BL, Bales CR, Shapiro MJ, Metzler MH, Conti VR, Baker CC, Bannon MP, Ochsner MG, Thomason MH, Hiatt JR, O’Malley K, Obeid FN, Gray P, Bankey PE, Knudson MM, Dyess DL, Enderson BL. Prospective study of blunt aortic injury: Multicenter Trial of the American Association for the Surgery of Trauma. J Trauma 1997;42:p374–380; discussion 380–383.
15. Estrera AL, Gochnour DC, Azizzadeh A, Miller CC 3rd, Coogan S, Charlton-Ouw K, Holcomb JB, Safi HJ. Progress in the treatment of blunt thoracic aortic injury: 12-year single-institution experience. Ann Thorac Surg 2010;90:64–71.
16. Bhaskar J, Foo J, Sharma AK. Clamp-and-sew technique for traumatic injuries of the aorta: 20-year experience. Asian Cardiovasc Thorac Ann 2010;18:161–165
17. von Oppell UO, Dunne TT, De Groot MK, Zilla P. Traumatic aortic rupture: twenty-year metaanalysis of mortality and risk of paraplegia. Ann Thorac Surg1994;58:585–593.
18. Cardarelli MG, McLaughlin JS, Downing SW, Brown JM, Attar S, Griffith BP. Management of traumatic aortic rupture: a 30-year experience. Ann Surg 2002;236: 465–469.
19. Azizzadeh A, Charlton-Ouw KM, Chen Z, Rahbar MH, Estrera AL, Amer H, Coogan SM, Safi HJ. An outcome analysis of endovascular versus open repair of blunt traumatic aortic injuries. J Vasc Surg 2013;57:108–114.
20. Durham CA, McNally MM, Parker FM, Bogey WM, Powell CS, Goettler CE, Rotondo MF, Stoner MC. A contemporary rural trauma center experience in blunt traumatic aortic injury. J Vasc Surg 2010;52:p884–889; discussion 889–890.
21. Forbes TL, Harris JR, Lawlor DK, Derose G. Aortic dilatation after endovascular repair of blunt traumatic thoracic aortic injuries. J Vasc Surg 2010;52:45–48.
22. Geisbusch P, Kotelis D,Weber TF, Hyhlik-Durr A, Bockler D. Endovascular repair of ruptured thoracic aortic aneurysms is associated with high perioperative mortality and morbidity. J Vasc Surg 2010;51:299–304.
23. Karmy-Jones R, Ferrigno L, Teso D, LongWB3rd, Shackford S. Endovascular repair compared with operative repair of traumatic rupture of the thoracic aorta: a nonsystematic review and a plea for trauma-specific reporting guidelines. J Trauma 2011;71:1059–1072.
24. Lang JL, Minei JP, Modrall JG, Clagett GP, Valentine RJ. The limitations of thoracic endovascular aortic repair in altering the natural history of blunt aortic injury. J Vasc Surg 2010;52:290–297; discussion 297.
25. Oberhuber A, Erhard L, Orend KH, Sunder-Plassmann L. Ten years of endovascular treatment of traumatic aortic transection: a single centre experience. Thorac Cardiovasc Surg 2010;58:143–147.
26. Rheaume P, Chen J, Casey P. Open vs endovascular repair of blunt traumatic thoracic aortic injuries. J Vasc Surg 2010;51:76376–9.
27. Riesenman PJ, Brooks JD, Farber MA. Acute blunt traumatic injury to the descending thoracic aorta. J Vasc Surg 2012;56:1274–1280.
28. Tong MZ, Koka P, Forbes TL. Economic evaluation of open vs endovascular repair of blunt traumatic thoracic aortic injuries. J Vasc Surg 2010;52:p31–38 e3.
29. Xenos ES, Bietz GJ, Davenport DL. Endoluminal versus open repair of descending thoracic aortic rupture: a review of the National Trauma Databank. Ther Adv Cardiovasc Dis 2011;5:221–225.
30. Erbel R, Bednarczyk I, Pop T, Todt M, Henrichs KJ, Brunier A, Thelen M, Meyer J.Detection of dissection of the aortic intima and media after angioplasty of coarctation of the aorta. An angiographic, computer tomographic, and echocardiographic comparative study. Circulation 1990;81:805–814.
31. 298. Piffaretti G, Mariscalco G, Tozzi M, Bruno VD, Sala A, Castelli P. Acute iatrogenictype A aortic dissection following thoracic aortic endografting. J Vasc Surg 2010; 51:993–999.
32. Leontyev S, Borger MA, Legare JF, Merk D, Hahn J, Seeburger J, Lehmann S, Mohr FW. Iatrogenic type A aortic dissection during cardiac procedures: early and late outcome in 48 patients. Eur J Cardiothorac Surg 2012;41:641–646.
33. Januzzi JL, Sabatine MS, Eagle KA, Evangelista A, Bruckman D, Fattori R, Oh JK, Moore AG, Sechtem U, Llovet A, Gilon D, Pape L, O’Gara PT, Mehta R, Cooper JV, Hagan PG, Armstrong WF, Deeb GM, Suzuki T, Nienaber CA, Isselbacher EM. Iatrogenic aortic dissection. Am J Cardio
34. BW Starnes, ZM Arthurs: Endovascular management of vascular trauma. Perspect Vasc Surg Endovasc Ther. 18 (2):114-129 2006
35. ME Giswold, GJ Landry, LM Taylor, et al.: Iatrogenic arterial injury is an increasingly important cause of arterial trauma. Am J Surg. 187 (5):590-592 2004 discussion 592–593
36. KG Elliott, AJ Johnstone: Diagnosing acute compartment syndrome. J Bone Joint Surg Br. 85 (5):625-632 2003
37. BH Yamane, G Tefera, JR Hoch, et al.: Blunt thoracic aortic injury: open or stent graft repair?. Surgery. 144 (4):575-580 2008 discussion 580–572
38. D Richens, K Kotidis, M Neale, et al.: Rupture of the aorta following road traffic accidents in the United Kingdom 1992–1999. The results of the co-operative crash injury study. Eur J Cardiothorac Surg. 23 (2):143-148 2003
39. N Kato, MD Dake, DC Miller, et al.: Traumatic thoracic aortic aneurysm: treatment with endovascular stent-grafts. Radiology. 205 (3):657-662 1997
40. DR Lebl, RA Dicker, DA Spain, et al.: Dramatic shift in the primary management of traumatic thoracic aortic rupture. Arch Surg. 141 (2):177-180 2006
41. BG Peterson, JS Matsumura, MD Morasch, et al.: Percutaneous endovascular repair of blunt thoracic aortic transection. J Trauma. 59 (5):1062-1065 2005
42. MM du, JA Reekers, R Balm, et al.: Collapse of a stent-graft following treatment of a traumatic thoracic aortic rupture. J Endovasc Ther. 12 (4):503-507 2005
43. FG Bakaeen, MJ Wall Jr, KL Mattox: Successful repair of an avulsion of the superior vena cava from the right atrium inflicted by blunt trauma. J Trauma. 59 (6):1486-1488 2005
44. KL Mattox, DV Feliciano, J Burch, et al.: Five thousand seven hundred sixty cardiovascular injuries in 4459 patients. Epidemiologic evolution 1958 to 1987. Ann Surg. 209 (6):698-705 1989 discussion 706–697
45. VK Mittal, TJ Paulson, E Colaiuta, et al.: Carotid artery injuries and their management. J Cardiovasc Surg (Torino). 41 (3):423-431 2000
46. TP Davis, DV Feliciano, GS Rozycki, et al.: Results with abdominal vascular trauma in the modern era. Am Surg. 67 (6):565-570 2001 discussion 570–561
47. WB McIntyre, JL Ballard: Cervicothoracic vascular injuries. Semin Vasc Surg. 11 (232)1998
48. AB van As, DF van Deurzen, EJ Verleisdonk: Gunshots to the neck: selective angiography as part of conservative management. Injury. 33 (5):453-456 2002
49. D Demetriades, JA Asensio, G Velmahos, et al.: Complex problems in penetrating neck trauma. Surg Clin North Am. 76 (4):661-683 1996
50. TM Duane, F Parker, GK Stokes, et al.: Endovascular carotid stenting after trauma. J Trauma. 52 (1):149-153 2002
51. JD McNeil, AC Chiou, MG Gunlock, et al.: Successful endovascular therapy of a penetrating zone III internal carotid injury. J Vasc Surg. 36 (1):187-190 2002
52. YH Tsai, HF Wong, HH Weng, et al.: Stent-graft treatment of traumatic carotid artery dissecting pseudoaneurysm. Neuroradiology. 52 (11):1011-1016 2010
53. D Maras, C Lioupis, G Magoufis, et al.: Covered stent-graft treatment of traumatic internal carotid artery pseudoaneurysms: a review. Cardiovasc Intervent Radiol. 29 (6):958-968 2006
54. J DuBose, G Recinos, PG Teixeira, et al.: Endovascular stenting for the treatment of traumatic internal carotid injuries: expanding experience. J Trauma. 65 (6):1561-1566 2008
55. WJ Bromberg, BC Collier, LN Diebel, et al.: Blunt cerebrovascular injury practice management guidelines: the Eastern Association for the Surgery of Trauma. J Trauma. 68 (2):471-477 2010
56. KG Moulakakis, S Mylonas, E Avgerinos, et al.: An update of the role of endovascular repair in blunt carotid artery trauma. Eur J Vasc Endovasc Surg. 40 (3):312-319 2010
57. JD Berne, A Cook, SA Rowe, et al.: A multivariate logistic regression analysis of risk factors for blunt cerebrovascular injury. J Vasc Surg. 51 (1):57-64 2010
58. WL Biffl, CC Cothren, EE Moore, et al.: Western Trauma Association critical decisions in trauma: screening for and treatment of blunt cerebrovascular injuries. J Trauma. 67 (6):1150-1153 2009
59. WL Biffl, EE Moore, PJ Offner, et al.: Blunt carotid arterial injuries: implications of a new grading scale. J Trauma. 47 (5):845-853 1999
60. NM Edwards, TC Fabian, JA Claridge, et al.: Antithrombotic therapy and endovascular stents are effective treatment for blunt carotid injuries: results from longterm followup. J Am Coll Surg. 204 (5):1007-1013 2007 discussion 1014–1005
61. Li W, D’Ayala M, Hirshberg A, et al: Comparison of conservative and operative treatment for blunt carotid injuries: analysis of the National Trauma Data Bank, J Vasc Surg 51(3):593–599, e592.
62. CC Cothren, WL Biffl, EE Moore, et al.: Treatment for blunt cerebrovascular injuries: equivalence of anticoagulation and antiplatelet agents. Arch Surg. 144 (7):685-690 2009
63. JG Tyburski, RF Wilson, C Dente, et al.: Factors affecting mortality rates in patients with abdominal vascular injuries. J Trauma. 50 (6):1020-1026 2001
64. JA Asensio, W Forno, G Roldan, et al.: Visceral vascular injuries. Surg Clin North Am. 82 (1):1-20 2002 xix
65. JS Paul, TP Webb, C Aprahamian, et al.: Intraabdominal vascular injury: are we getting any better?. J Trauma. 2010
66. JA Asensio, S Chahwan, D Hanpeter, et al.: Operative management and outcome of 302 abdominal vascular injuries. Am J Surg. 180 (6):528-533 2000 discussion 533–524
67. P Rhee, E Koustova, HB Alam: Searching for the optimal resuscitation method: recommendations for the initial fluid resuscitation of combat casualties. J Trauma. 54 (5 Suppl):S52-S62 2003
68. HP Santry, HB Alam: Fluid resuscitation: past, present, and the future. Shock. 33 (3):229-241 2010
69. JA Asensio, P Petrone, G O’Shanahan, et al.: Managing exsanguination: what we know about damage control/bailout is not enough. Proc (Bayl Univ Med Cent). 16 (3):294-296 2003
70. K Inaba, AW Kirkpatrick, J Finkelstein, et al.: Blunt abdominal aortic trauma in association with thoracolumbar spine fractures. Injury. 32 (3):201-207 2001
71. X Ding, J Jiang, Q Su, et al.: Endovascular stent graft repair of a penetrating aortic injury. Ann Thorac Surg. 90 (2):632-634 2010
72. MW Yeh, JK Horn, WP Schecter, et al.: Endovascular repair of an actively hemorrhaging gunshot injury to the abdominal aorta. J Vasc Surg. 42 (5):1007-1009 2005
73. ZM Arthurs, VY Sohn, BW Starnes: Vascular trauma: endovascular management and techniques. Surg Clin North Am. 87 (5):1179-1192 2007 x–xi
74. BC Reuben, MG Whitten, M Sarfati, et al.: Increasing use of endovascular therapy in acute arterial injuries: analysis of the National Trauma Data Bank. J Vasc Surg. 46 (6):1222-1226 2007
75. JA Asensio, JD Berne, S Chahwan, et al.: Traumatic injury to the superior mesenteric artery. Am J Surg. 178 (3):235-239 1999
76. JA Asensio, LD Britt, A Borzotta, et al.: Multiinstitutional experience with the management of superior mesenteric artery injuries. J Am Coll Surg. 193 (4):354-365 2001 discussion 365–356
77. T Patel, I Kuladhipati, S Shah: Successful percutaneous endovascular management of acute post-traumatic superior mesenteric artery dissection using a transradial approach. J Invasive Cardiol. 22 (4):E61-E64 2010
78. JA Asensio, P Petrone, L Garcia-Nunez, et al.: Superior mesenteric venous injuries: to ligate or to repair remains the question. J Trauma. 62 (3):668-675 2007 discussion 675
79. JK Smith, PJ Kenney: Imaging of renal trauma. Radiol Clin North Am. 41 (5):1019-1035 2003
80. LM Bruce, MA Croce, JM Santaniello, et al.: Blunt renal artery injury: incidence, diagnosis, and management. Am Surg. 67 (6):550-554 2001 discussion 555–556
81. A Tillou, J Romero, JA Asensio, et al.: Renal vascular injuries. Surg Clin North Am. 81 (6):1417-1430 2001
82. JT Lee, RA White: Endovascular management of blunt traumatic renal artery dissection. J Endovasc Ther. 9 (3):354-358 2002
83. JA Asensio, L McDuffie, P Petrone, et al.: Reliable variables in the exsanguinated patient which indicate damage control and predict outcome. Am J Surg. 182 (6):743-751 2001
84. JA Asensio, P Petrone, G Roldan, et al.: Analysis of 185 iliac vessel injuries: risk factors and predictors of outcome. Arch Surg. 138 (11):1187-1193 2003 discussion 1193–1184
85. JT Lee, FS Bongard: Iliac vessel injuries. Surg Clin North Am. 82 (1):21-48 2002 xix
86. M Kiguchi, HJ O’Rourke, A Dasyam, et al.: Endovascular repair of 2 iliac pseudoaneurysms and arteriovenous fistula following spine surgery. Vasc Endovascular Surg. 44 (2):126-130 2010
87. SP Lyden, SD Srivastava, DL Waldman, et al.: Common iliac artery dissection after blunt trauma: case report of endovascular repair and literature review. J Trauma. 50 (2):339-342 2001
88. J Kuehne, J Frankhouse, G Modrall, et al.: Determinants of survival after inferior vena cava trauma. Am Surg. 65 (10):976-981 1999
89. RF Buckman, AS Pathak, MM Badellino, et al.: Injuries of the inferior vena cava. Surg Clin North Am. 81 (6):1431-1447 2001
90. V Formisano, A Di Muria, G Muto, et al.: Inferior vena cava gunshot injury: case report and a review of the literature. Ann Ital Chir. 77 (2):173-177 2006
91. RF Buckman, AS Pathak, MM Badellino, et al.: Portal vein injuries. Surg Clin North Am. 81 (6):1449-1462 2001
92. EH Carrillo, DA Spain, FB Miller, et al.: Femoral vessel injuries. Surg Clin North Am. 82 (1):49-65 2002
93. PH Lin, AJ Koffron, PJ Guske, et al.: Penetrating injuries of the subclavian artery. Am J Surg. 185 (6):580-584 2003
94. D Demetriades, JA Asensio: Subclavian and axillary vascular injuries. Surg Clin North Am. 81 (6):1357-1373 2001 xiii
95. EH Phillips, WF Rogers, MR Gaspar: First rib fractures: incidence of vascular injury and indications for angiography. Surgery. 89 (1):42-47 1981
96. DF du Toit, DC Strauss, M Blaszczyk, et al.: Endovascular treatment of penetrating thoracic outlet arterial injuries. Eur J Vasc Endovasc Surg. 19 (5):489-495 2000
97. ES Xenos, M Freeman, S Stevens, et al.: Covered stents for injuries of subclavian and axillary arteries. J Vasc Surg. 38 (3):451-454 2003
98. CE Fields, R Latifi, RR Ivatury: Brachial and forearm vessel injuries. Surg Clin North Am. 82 (1):105-114 2002
99. KR Borman, WH Snyder 3rd, JA Weigelt: Civilian arterial trauma of the upper extremity. An 11 year experience in 267 patients. Am J Surg. 148 (6):796-799 1984
100. JA Asensio, EJ Kuncir, LM Garcia-Nunez, et al.: Femoral vessel injuries: analysis of factors predictive of outcomes. J Am Coll Surg. 203 (4):512-520 2006
101. J Meyer, J Walsh, J Schuler, et al.: The early fate of venous repair after civilian vascular trauma. A clinical, hemodynamic, and venographic assessment. Ann Surg. 206 (4):458-464 1987
102. PS Mullenix, SR Steele, CA Andersen, et al.: Limb salvage and outcomes among patients with traumatic popliteal vascular injury: an analysis of the National Trauma Data Bank. J Vasc Surg. 44 (1):94-100 2006
103. ER Frykberg: Popliteal vascular injuries. Surg Clin North Am. 82 (1):67-89 2002
104. VL Rowe, A Salim, J Lipham, et al.: Shank vessel injuries. Surg Clin North Am. 82 (1):91-104 2002 xx
105. WH Wagner, ER Calkins, FA Weaver, et al.: Blunt popliteal artery trauma: one hundred consecutive injuries. J Vasc Surg. 7 (5):736-743 1988
106. WH Wagner, AE Yellin, FA Weaver, et al.: Acute treatment of penetrating popliteal artery trauma: the importance of soft tissue injury. Ann Vasc Surg. 8 (6):557-565 1994
107. SK Bains, PA Vlachou, HS Rayt, et al.: An observational cohort study of the management and outcomes of vascular trauma. Surgeon. 7 (6):332-335 2009
108. PA Vagefi, CJ Kwolek, S Wicky, et al.: Congestive heart failure from traumatic arteriovenous fistula. J Am Coll Surg. 209 (1):150 2009
109. Reed, JK Thompson, CJ Crafton, et al.: Timing of endovascular repair of blunt traumatic thoracic aortic transections. J Vasc Surg. 43 (4):684-688 2006
110. C Thalhammer, AS Kirchherr, F Uhlich, et al.: Postcatheterization pseudoaneurysms and arteriovenous fistulas: repair with percutaneous implantation of endovascular covered stents. Radiology. 214 (1):127-131 2000
111. R Gandini, A Ippoliti, E Pampana, et al.: Emergency endograft placement for recurrent aortocaval fistula after conventional AAA repair. J Endovasc Ther. 9 (2):208-211 2002
112. W Zhou, RL Bush, TT Terramani, et al.: Treatment options of iatrogenic pelvic vein injuries: conventional operative versus endovascular approach–case reports. Vasc Endovascular Surg. 38 (6):569-573 2004
113. DB Klinkner, MJ Arca, BD Lewis, et al.: Pediatric vascular injuries: patterns of injury, morbidity, and mortality. J Pediatr Surg. 42 (1):178-182 2007 discussion 182–173
114. SR Shah, PD Wearden, BA Gaines: Pediatric peripheral vascular injuries: a review of our experience. J Surg Res. 153 (1):162-166 2009
115. P Mommsen, C Zeckey, F Hildebrand, et al.: Traumatic extremity arterial injury in children: epidemiology, diagnostics, treatment and prognostic value of Mangled Extremity Severity Score. J Orthop Surg Res. 5:25 2010
116. RB Chamoun, ME Mawad, WE Whitehead, et al.: Extracranial traumatic carotid artery dissections in children: a review of current diagnosis and treatment options. J Neurosurg Pediatr. 2 (2):101-108 2008
117. G Barmparas, K Inaba, P Talving, et al.: Pediatric vs adult vascular trauma: a National Trauma Databank review. J Pediatr Surg. 45 (7):1404-1412 2010